Clinical Case Analysis of Esophageal Malignant Glomus Tumor Diagnosed by MSCT
-
摘要:
食管恶性血管球瘤罕见,临床特征及影像学表现缺乏特异性,术前鉴别诊断困难,影响临床治疗决策。本文报道 1 例我院收治的食管恶性血管球瘤术后6年肝内多发转移的患者,回顾性分析该病例的临床资料及影像学表现,旨在提高影像科医师对食管血管球瘤CT表现的认识,为临床诊治提供帮助。
Abstract:Esophageal malignant glomus tumors are rare, and their clinical features and imaging manifestations lack specificity. Preoperative differential diagnosis is difficult, which affects clinical treatment decisions. This article reports a case of a patient with multiple intrahepatic metastases of esophageal malignant glomus tumor admitted to our hospital six years after surgery. The clinical data and imaging findings of this case were retrospectively analyzed to improve the understanding of CT manifestations of esophageal glomus tumors by radiologists and provide assistance for clinical diagnosis and treatment.
-
Keywords:
- tomography /
- X-ray computed /
- glomus tumor /
- esophagus
-
血管球瘤(glomus tumor,GT)是由类似正常血管球变异平滑肌细胞组成的,相对少见的间叶源性肿瘤,好发于甲床下、手掌、手腕和足底富含血管球的真皮或皮下组织[1],罕见于胃、气管、乳头、胸壁等部位[2-5],发生于食管的GT极为罕见[6]。大多数GT呈良性,恶性GT仅占所有GT的不到1%[7]。1924年,Mason首次从组织学层面对GT进行了描述[8],迄今为止国内外有关食管GT的文献报道不足25例,且均以病理和临床分析为主,简要提及影像学表现,术前CT检查能够对GT的位置、形态、大小、内部结构、生长方式及血供、其与邻近结构的关系、有无邻近转移等进行无创评估,对临床诊断和治疗具有重要意义。本文我们报道了1例恶性食管GT术后,肝脏多发转移的病例,就该病例CT表现做较详细的描述,以提高影像科及临床医师对该疾病CT表现的认识,为临床诊断及为患者提供个体化的治疗提供帮助。
1. 病例资料
1.1 临床资料及相关检查
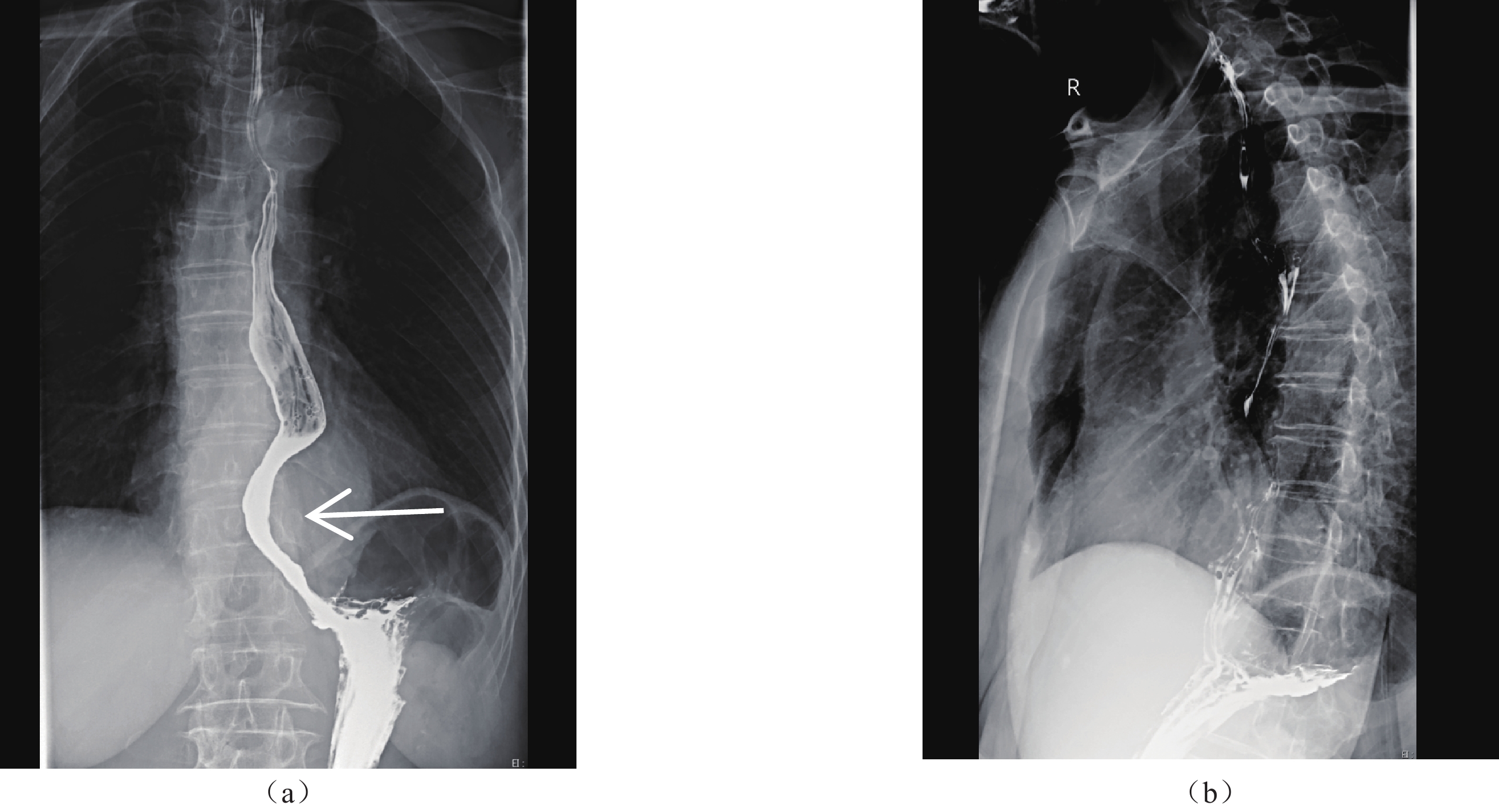
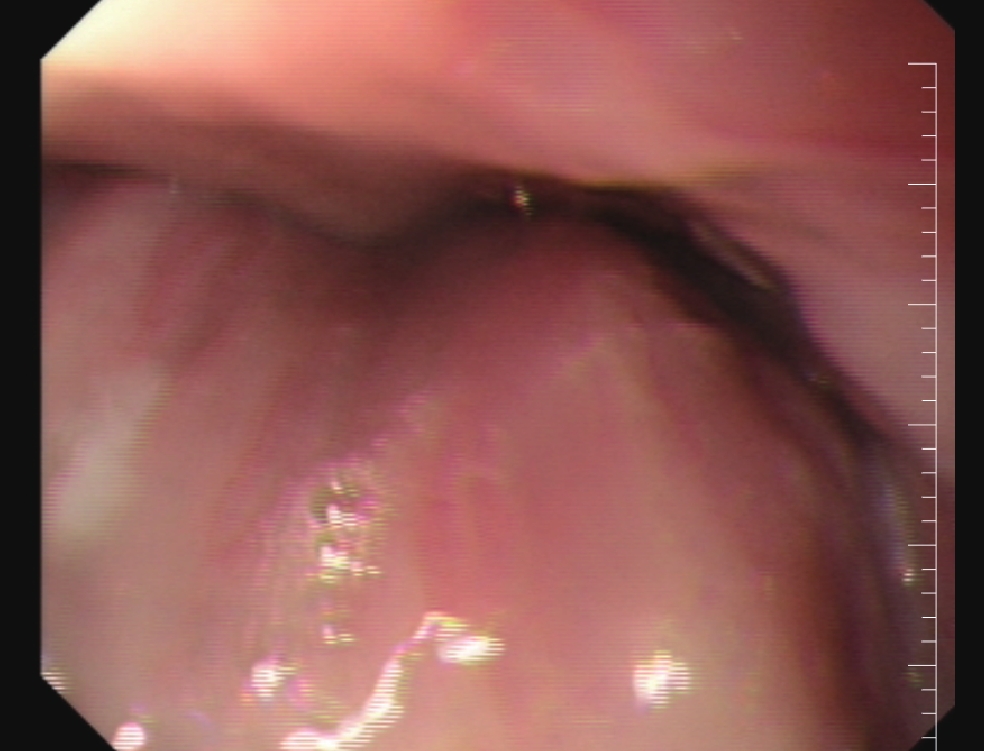
患者,女,74岁 ,近1月来无明显诱因出现进食梗阻,无胸痛、反酸、恶心、呕吐及体重减轻等症状,发病后未行特殊诊治,后梗阻逐渐加重,遂入我院就诊。入院后电子胃镜示下段食管隆起性病变(图1)。超声内镜检查提示食管下段黏膜下肌层外生性不均质肿块。肿瘤标志物:糖类抗原72-4 7.48 ↑(正常参考值:0~6.9 U/ml);神经元特异性烯醇化酶 19.28 ↑(正常参考值:0.00~16.30 ng/mL)。上消化道造影:食管下段胸11-12椎体水平外压性改变(图2)。
![]() 图 2 上消化道造影图像注:图2上消化道造影充盈像(a),食管下段胸11-12椎体水平外压性改变。上消化道造影黏膜像(b)黏膜光滑,未见增粗和中断。Figure 2. Gastroenterography image
图 2 上消化道造影图像注:图2上消化道造影充盈像(a),食管下段胸11-12椎体水平外压性改变。上消化道造影黏膜像(b)黏膜光滑,未见增粗和中断。Figure 2. Gastroenterography image1.2 MSCT检查
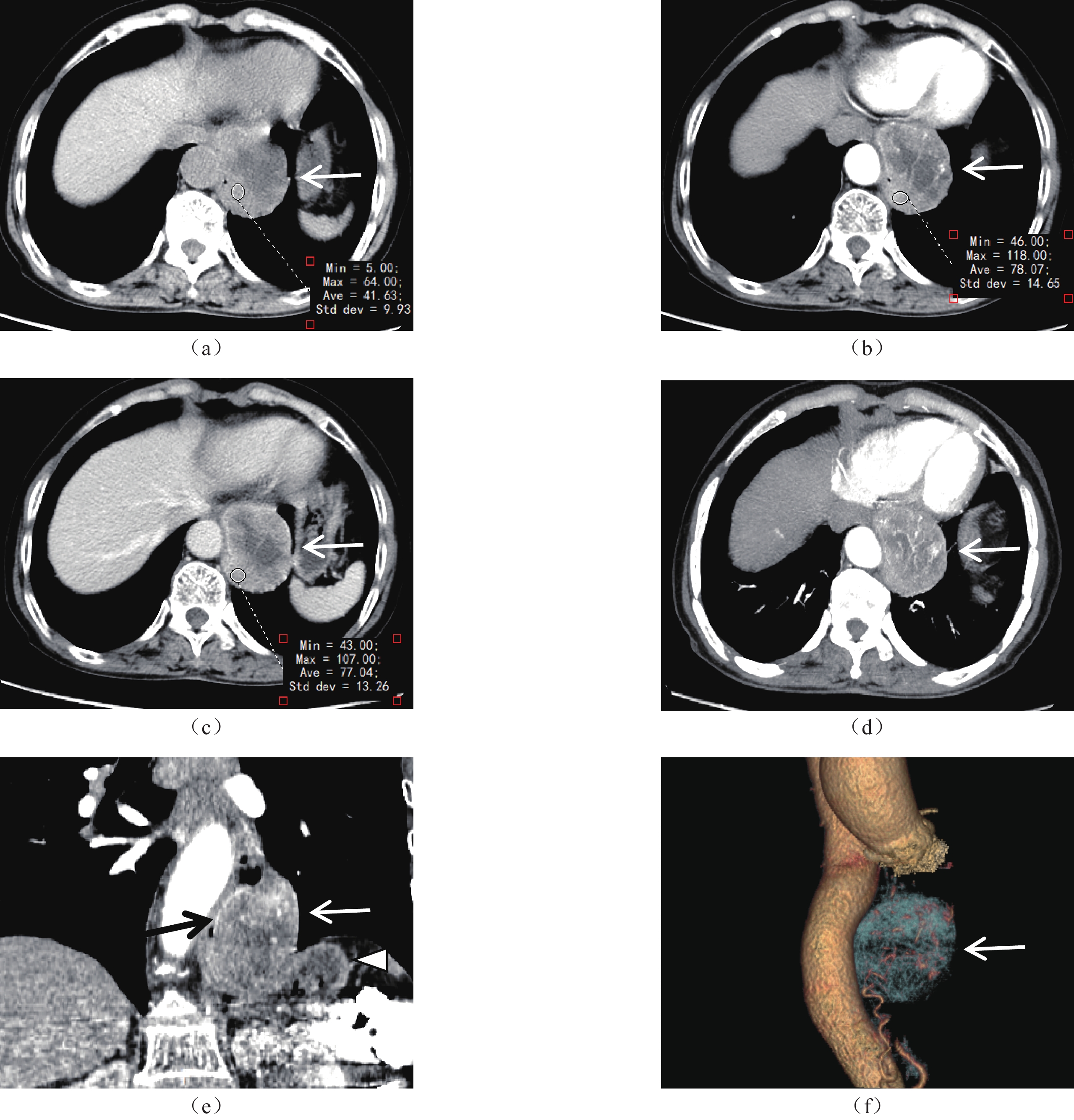
胸部CT平扫:左后下纵隔食管下段后外侧见外生性团块状占位,大小约4.2 cm×5.5 cm×6.8 cm,密度不均,以软组织密度为主,平均CT值约41.6 HU,中心可见斑片状低密度区,边界较清楚,食管下段受压明显,病灶同时向下压迫胃底,毗邻胸主动脉,中上段食管扩张不明显。纵隔及肝胃间隙未见肿大淋巴结。胸部增强扫描左后下纵隔食管下段后外侧病灶由胃左动脉供血,中度不均匀持续强化,内见多发细小血管影穿行,病灶实性部分动脉期平均CT值约78.1 HU,静脉期平均CT值约77.0 HU,且静脉期强化范围较动脉期增大;病灶中心低密度区边缘可见轻度强化,食管黏膜可见强化(图3)。
1.3 病理诊断
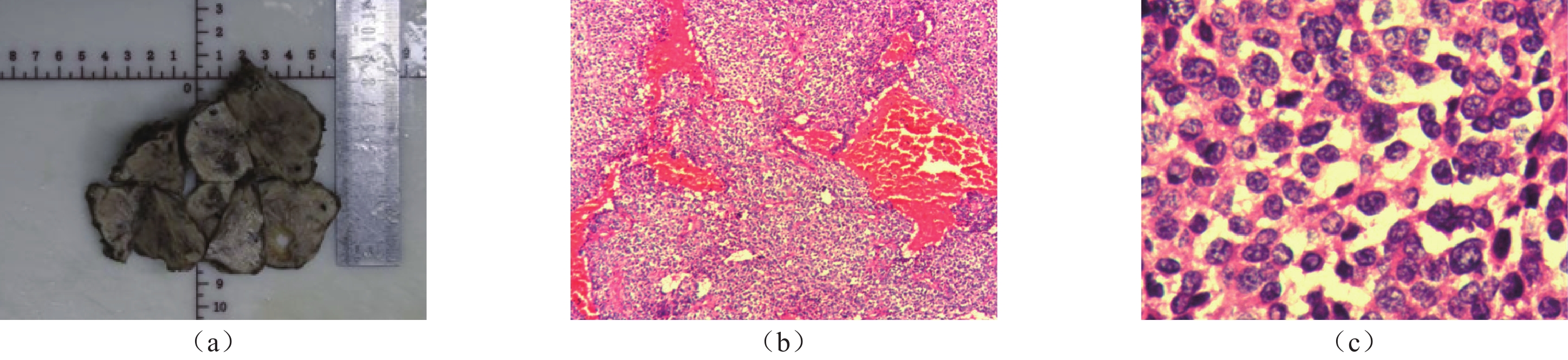
全麻下行食管下段肿瘤切除术,术后病理检查(图4)。大体病理:灰白结节样肿物一个,大小6 cm×5 cm×5 cm,表面未见明显包膜,多切面切开灰白、实性、质中,较韧,可见散在点状暗红色区,部分区域有粘液变性。镜下改变:瘤细胞丰富,由形态较一致的短梭形细胞至卵圆形细胞组成,胞质淡染透明状或呈淡嗜伊红色,细胞边界尚清,部分区域呈实性巢团状,部分区域呈条束状排列,瘤细胞分布于大小不一的血管周围,其内可见丰富的血管,呈分支状或鹿角状,呈血管外皮瘤样结构,部分瘤细胞有明显异型性,细胞核深染,可见核分裂象 > 5个/50 HPF, 瘤内可见平滑肌束,瘤细胞与平滑肌细胞有移行,部分间质伴有粘液变性。免疫组化:CK(−),Vim(+),SMA(+),H-caldesmon(+),calponin(部分+),Syn(部分+),Bcl-2(+),S-100(−),CD117(−),CD34(−),Dog-1(−),Ki67阳性细胞数10。
1.4 治疗
经完善术前相关检查,患者于我院行全麻下食管下段肿瘤切除术,术中见肿瘤位于食管下段,约6 cm×5 cm×4 cm大小,形状不规则,包膜完整,位于食管下段肌层内,与食管粘膜关系紧密。术后患者1周出现食管瘘,完善相关术前准备后,再次行硬膜外麻醉下空肠造口术,术后患者恢复良好。
1.5 随访
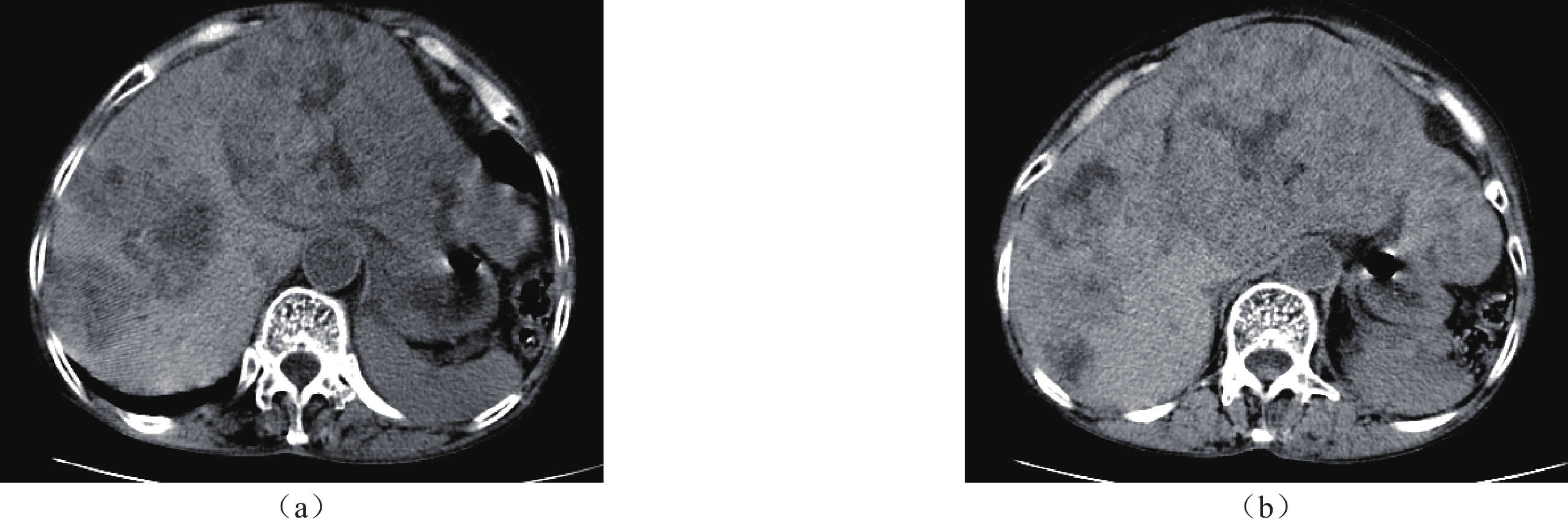
患者术后未进行放化疗,于术后第6年,因腹痛、腹胀入院,行腹部超声及CT平扫示肝脏多发占位,结合病史,考虑转移瘤可能(图5)。
2. 讨论
2.1 临床特征
良性GT最常见的部位是四肢远端浅表软组织,而恶性GT则更常出现在深部软组织和内脏,且发病年龄谱广泛,更好发于食管;与胃的GT不同,报道的食管GT中亦以恶性居多[9]。笔者认为这可能与食管良性GT较小,没有临床症状,往往内镜体检中才能被发现有关。食管恶性GT临床缺乏特异性,多为吞咽困难、体重减轻,亦有便血、呼吸困难及声音嘶哑的报道[1,10-11]。
2.2 病理学及分子遗传特征
GT细胞学特征在肿瘤内部和肿瘤之间差异很大,从良性GT中均一的上皮样瘤细胞,到显著的梭形细胞形态及明显的异型性;低倍镜常见被纤维组织分隔的以扩张小血管为中心的上皮样瘤细胞巢团[6,12]。免疫组化:SMA、vimentin、Ⅳ型胶原表达阳性。目前,食管恶性GT的诊断标准存在争议,多数学者则参照2001年由Folpe等[13]提出的四肢软组织恶性GT的诊断标准:①肿瘤位置深且最大径>2 cm;②可见非典型核分裂象;③肿瘤细胞核呈中~高度异型,核分裂象≥5个/50 HPF;上述条件的组合。
Birkness-Gartman[6]等报道9例恶性食管GT中有5例具有分子遗传学信息,均表现为各种NOTCH1/2/3基因的改变,Pancsa等[9]认为发现NOTCH1/2/3基因的重组可明确GT诊断。另有一小部分恶性GT显示BRAF突变,这增加了靶向治疗的可能性。
2.3 CT表现
虽然,既往食管GT的病例报道中,仅有少数报道简要提及CT表现,然而,胃作为胃肠道GT最常见发病部位[14],已有不少学者对其影像学表现进行研究、归纳。研究发现胃的GT的CT表现为:①良性者常<2 cm,胃黏膜下,边界清晰,等密度结节,可以向腔内、腔外或混合性生长,增强扫描动脉期均匀或不均匀明显强化,静脉期渐进性强化,即静脉期强化率较动脉期高,并认为渐进性强化方式与肿瘤内部富含血管及纤维组织有关;②恶性GT则表现为,肿瘤较大,边界不清,形态不规则,内部因坏死、囊变密度不均,增强扫描囊性部分不强化,实性部分动脉期不均匀明显强化,静脉期强化与动脉期强化表现相似[15-16]。
Marcella[17]等报道了一例因体检偶然发现的中段食管的良性GT,长径<2 cm,病灶密度均匀,边缘清晰,向腔内突出,增强CT显示结节渐进性均匀强化,与上述胃良性GT报道一致;本例食管恶性GT表现为食管下段外生性不均匀较大软组织密度肿块,内见低密度区,动脉期实性部分中度不均匀强化,静脉期持续性强化,即动脉期强化率与静脉期强化率相仿,中心低密度区静脉期边缘强化,结合病理病灶内存在间质粘液变性,推测为粘液成分吸附造影剂所致,与上述胃恶性GT实性部分明显强化,病灶中心坏死、囊变有所不同,但是本病例动脉期显示病灶内部多发强化细小血管影,并由腹腔干分支动脉供血,说明肿块血供较丰富。
笔者通过复习国内外食管GT的相关文献,发现食管GT常发生于中下段食管黏膜下,并与胃的GT不同,食管GT以恶性居多,肿块较大,内可因黏液变性、坏死及囊变等密度不均,并常出现纵隔淋巴结、肺、胸膜转移,也可转移至头皮、骨关节、心包等部位。值得注意的是,肿瘤常位于后纵隔,具有侵袭性,影像科医生应注意观察病灶与邻近组织器官的关系,尤其是主动脉,以便提示手术难度及风险;Birkness-Gartman等[6]报道一例食管GT与主动脉粘连,术后出现食管-主动脉瘘,最终导致大出血而死亡的病例。
2.4 鉴别诊断
食管GT需要与发生于食管黏膜下且血供较丰富软组织肿瘤进行鉴别,主要包括食管间质瘤、血管瘤、神经内分泌肿瘤等。①食管间质瘤:好发于中下段食管,肿块较大,均匀等或稍低密度,轻度强化[18],与食管恶性GT不均匀中度强化可以鉴别。②血管瘤:食管血管瘤罕见,良性,富血供,若发现静脉石,有助于与GT的鉴别。③神经内分泌肿瘤:好发于中下段食管,食管壁增厚,病灶长轴与食管平行,增强扫描持续性明显均匀不均匀强化[19]。④食管癌:当食管GT突破黏膜,出现溃疡、呈多结节表现时,需要与食管癌鉴别,食管癌强化不及GT明显。
2.5 治疗及预后
食管GT最佳的治疗方法尚不明确,目前多采取手术治疗,手术方式依赖于临床医生的经验及专业知识,术后可以联合放化疗、免疫治疗、靶向治疗等。因肿瘤具有侵袭性,易发生转移,预后较差,不少学者建议采用多学科专家团队共同探讨管理模式,为患者提供个体化治疗方案。
3. 结论
食管GT的恶性居多,增强CT扫描时当发现食管中下段较大不均匀软组织密度占位,持续性中度强化,应考虑到GT的可能。病理学及免疫组化仍是诊断食管GT的金标准。食管GT具有侵袭性,预后较差,易发生淋巴结转移及远处转移,应尽可能多学科专家团队共同参与,制定最优的个体化治疗。
-
图 2 上消化道造影图像
注:图2上消化道造影充盈像(a),食管下段胸11-12椎体水平外压性改变。上消化道造影黏膜像(b)黏膜光滑,未见增粗和中断。
Figure 2. Gastroenterography image
-
[1] BALI G S, HARTMAN D J, HAIGHT J B, et al. A rare case of malignant glomus tumor of the esophagus[J]. Case Reports in Oncology Medicine, 2013, 2013: 287078. DOI: 10.1155/2013/287078.
[2] SHE C, PENG J, LI Y, et al. Endoscopic-guided therapy for tracheal glomus tumor: A case report on radiofrequency plasma-assisted therapy[J]. Ear Nose Throat J, 2024: 1580017984. DOI: 10.1177/01455613241272640
[3] ENGLE J A, DIBB J T, KUNDU S, et al. Glomus tumor of the chest wall with metastases to lung[J]. Cureus, 2024, 16(9): e69122. DOI: 10.7759/cureus.69122.
[4] MOHAMED W T, JAHAGIRDAR V, JABER F, et al. Glomus tumor of the stomach presenting with upper gastrointestinal bleeding: A case report[J]. Journal of Investigative Medicine High Impact Case Reports, 2023, 11: 1626040635. DOI: 10.1177/23247096231192891.
[5] AL-ISHAQ Z, ASIF U, ROY M, et al. Glomus tumour of the nipple in a male patient[J]. Annals of the Royal College of Surgeons of England, 2022, 104(3): e60-e63. DOI: 10.1308/rcsann.2021.0141.
[6] BIRKNESS-GARTMAN J E, WANGSIRICHAROEN S, LAZAR A J, et al. Oesophageal glomus tumours: rare neoplasms with aggressive clinical behaviour[J]. Histopathology, 2023, 82(7): 1048-1055. DOI: 10.1111/his.14888.
[7] SUN Z, SUN F, YU C, et al. Malignant glomus tumor of prostate: A case report[J]. Front Oncol, 2023, 13: 1121307. DOI: 10.3389/fonc.2023.1121307.
[8] MASON F C. Angiomata of palate[J]. Proceedings of the Royal Society of Medicine , 1924, 17(Laryngol Sect): 49
[9] PANCSA T, MARTÍNEK P, MICHAL M. Malignant esophageal glomus tumor with carmn: notch2 fusion: An additional tumor underscoring the frequent tendency of esophageal glomus tumors for aggressive behavior[J]. International Journal of Surgical Pathology , 2024: 104911761. DOI: 10.1177/10668969241291887
[10] UGRAS N, YERCİ ö, YALçıNKAYA U, et al. Malignant glomus tumor with oncocytic features: an unusual presentation of dysphagia[J]. Acta Pathologica, Microbiologica et Immunologica Scandinavica, 2015, 123(7): 613-617. DOI: 10.1111/apm.12394.
[11] XIAO A, AHLERS M, DRY S M, et al. Rare malignant glomus tumor of the esophagus with pulmonary metastasis: a case report[J]. AME Case Rep, 2022, 6: 20. DOI: 10.21037/acr-21-72.
[12] LIN J, SHEN J, YUE H, et al. Gastric glomus tumor: A clinicopathologic and immunohistochemical study of 21 cases[J]. BioMed Research International, 2020, 2020: 5637893. DOI: 10.1155/2020/5637893.
[13] FOLPE A L, FANBURG-SMITH J C, MIETTINEN M, et al. Atypical and malignant glomus tumors: Analysis of 52 cases, with a proposal for the reclassification of glomus tumors[J]. The American Journal of Surgical Pathology, 2001, 25(1): 1-12. DOI: 10.1097/00000478-200101000-00001.
[14] ROSSI U G, RUTIGLIANI M, PAPARO F, et al. Gastric glomus tumor: Endoscopy, MD-CT and pathologic features[J]. Gastroenterol Hepatol, 2021, 44(1): 35-36. DOI: 10.1016/j.gastrohep.2020.03.006.
[15] 赵帅, 刘译阳, 梁盼, 等. 胃肠血管球瘤的影像表现及临床病理分析[J]. 放射学实践, 2023, 38(6): 673-678 DOI: 10.1016/j.gastrohep.2020.03.006. ZHAO S, LIU Y Y, LIANG P, et al. Imaging manifestations and clinicopathological analysis of gastrointestinal glomus tumor[J]. Practical Radiology, 2023, 38(6): 673-678. DOI: 10.1016/j.gastrohep.2020.03.006.
[16] XING J J, HUANG W P, WANG F, et al. Computed tomography features and clinicopathological characteristics of gastric glomus tumor[J]. BMC Gastroenterology, 2022, 22(1): 1-7 DOI: 10.1186/s12876-021-02073-0.
[17] MARCELLA C, SHI R, YU T, et al. Asymptomatic esophageal glomus tumor: case report[J]. Journal of Gastrointestinal Oncology, 2019, 10(5): 1015-1020. DOI: 10.21037/jgo.2019.05.08.
[18] SHINAGARE A B, ZUKOTYNSKI K A, KRAJEWSKI K M, et al. Esophageal gastrointestinal stromal tumor: report of 7 patients[J]. Cancer Imaging, 2012, 12(1): 100-108. DOI: 10.1102/1470-7330.2012.0017.
[19] 王慧, 雷丽敏, 郭晓旭, 等. 食管神经内分泌肿瘤的临床影像表现分析[J]. 中国临床医学影像杂志, 2023, 34(9): 654-658. DOI: 10.12117∕jccmi.2023.09.009 WANG H, LEI L M, GUO X X, et al. Clinical and imaging analysis of esophageal neuroendocrine tumor[J]. The Chinese Journal of Clinical Medical Imaging2023, 34(9): 654-658. DOI:10.12117∕jccmi.2023.09.009(in Chinese).



 下载:
下载: