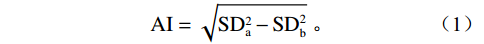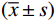Orthopedic Metal Artifact Reduction Combined with Iterative Reconstruction in CT Imaging after Lumbar Internal Fixation
-
摘要:
目的:探讨金属伪影抑制技术(O-MAR)联合迭代算法对腰椎内固定术后患者CT图像质量的影响,为术后效果评估提供准确依据。方法:回顾性分析20例行腰椎内固定术后CT检查,使用O-MAR和滤波反投影算法、iDose4重建骨算法图像(iDose4-1~7级)及软组织算法图像(iDose4-1~6级)。重组螺钉显示最佳的横断面和矢状面的骨算法图像及螺钉显示最佳及螺钉区域内椎间盘正中层面的横断面软组织算法图像,测量骨质和肌肉的噪声值(SD)并计算伪影指数(AI)。由两名放射科医师对骨及软组织算法图像的金属伪影抑制和诊断信息显示两方面分别评分。对主客观评价指标进行两组间比较和组间多重比较。结果:骨算法图像:使用O-MAR的图像SD、AI显著低于未使用的图像,不同等级iDose4图像的AI值随等级升高而逐渐降低;O-MAR图像金属伪影主观分显著提高,且iDose4-5~7评分高于FBP及iDose4-1~2;使用O-MAR时诊断信息评分显著提高,iDose4-2~4评分高于FBP及其他迭代等级,且iDose4-3为最佳。软组织算法图像:使用O-MAR的图像SD、AI低于未使用的图像;使用O-MAR的图像金属伪影评分高于未使用,诊断信息评分未使用O-MAR高于使用;对不同迭代等级,无论是否使用O-MAR,图像伪影和诊断信息评分均无差异。结论:建议联合使用O-MAR技术及中间迭代等级iDose4-3重建骨算法图像;软组织算法图像重建时不推荐使用迭代算法,建议同时重建使用和不使用O-MAR的图像以便配合观察。
Abstract:Objective: Exploring the effect of metal artifact reduction (O-MAR) technology combined with iterative algorithms on the computed tomography (CT) image quality of patients after lumbar spine internal fixation surgery, to provide an accurate basis for postoperative effect evaluation. Methods: CT images were collected from 20 patients who underwent lumbar spine internal fixation surgery. Using O-MAR, filtered back projection (FBP), and iDose4 algorithms, bone (iDose4-1~7 levels) and soft tissue images (iDose4-1~6 levels) were reconstructed. Screws were displayed the best in transverse and sagittal bone reconstructed images. The screw area (center plane) of the transverse soft tissue images of the intervertebral disc was also reconstructed. Noise levels in standard deviation (SD) of bone and muscle were measured, and the artifact index (AI) was calculated. Two radiologists separately rated the metal artifact suppression and diagnostic information in the bone and soft tissue images. The subjective and objective evaluation indicators of the two groups were compared, conducting multiple comparisons between groups. Statistical analyses were further performed on subjective and objective evaluation indicators, including O-MAR comparisons and/or multiple comparisons between groups with different levels of iDose4. Results: In the bone images, the SD and AI of images using O-MAR were significantly lower than those without O-MAR, and the AI values of iDose4 images at different levels gradually decreased as the dose level increased. The subjective score of metal artifacts in O-MAR images significantly improved, and the score of iDose4-5~7 was higher than those of filtered back projection (FBP) and iDose4-1~2. With O-MAR, the diagnostic information score significantly improved. The score of iDose4-2~4 was higher than that of FBP and other iterative levels, with iDose4-3 being the best. In soft tissue images, the SD and AI of images using O-MAR were lower than those without O-MAR. The metal artifact score of images using O-MAR was higher than that of images without, but the diagnostic information score of images not using O-MAR was higher than that of images with O-MAR; For different iteration levels, regardless of whether O-MAR was used or not, no difference was observed in image artifacts and diagnostic information scores. Conclusions: We suggest combining O-MAR technology with intermediate iteration level iDose4-3 for bone image reconstruction. The use of iterative algorithms for image reconstruction using soft-tissue algorithms is not recommended. The images with and without O-MAR should be simultaneously reconstructed for comparative observations.
-
Keywords:
- iterative algorithm /
- image quality /
- O-MAR /
- subjective evaluation /
- artifact index
-
腰椎内固定术是临床常见的金属植入物手术,广泛应用于腰椎间盘突出、滑脱、骨折等腰椎病变的外科治疗,常需放置金属螺钉进行内固定[1]。患者术后通常需行CT检查来评估手术效果和螺钉附近骨质以及椎间盘、椎管、附近软组织的情况。但常规CT图像金属植入物附近会产生明显伪影,严重影响邻近组织结构的显示。金属伪影抑制(orthopedic metal artifact reduction, O-MAR)技术是一种基于线性内插算法的图像重建技术,也是首个临床诊疗用骨科去金属伪影技术,可有效减轻金属等高原子序数植入物所产生的伪影[2]。
第4代迭代重建算法(the fourth generation iterative reconstruction algorithm, iDose4)是一种基于传统滤波反投影算法(filtered back projection, FBP)的重建技术[3],能将获得的图像数据构造多噪声模型和解剖模型,在重复迭代过程中剔除噪声数据,提高图像质量[4−5]。
本研究探讨O-MAR联合不同等级iDose4对腰椎内固定术后患者CT图像伪影抑制和诊断信息显示的影响,旨在获取骨及软组织算法图像重建的最佳参数组合,为临床术后效果评估提供准确依据。
1. 材料与方法
1.1 实验设备和一般资料
使用Philips IQon Spectral CT扫描仪和Philips星云工作站(IntelliSpace Portal,ISP)。随机收集2022年1月至2022年3月间行腰椎内固定术后CT检查的患者20例,男性10例,女性10例,平均年龄(60.1±2.04)岁。
纳入患者BMI范围在18~24,并排除既往曾行腰椎其他类型手术的患者。
1.2 图像采集
1.2.1 患者准备和扫描参数
患者仰卧于检查床,双臂上举,椎体与床面平行并置于扫描野中心。所有病例均为平扫,扫描范围第12胸椎至第1骶椎,扫描视野(field of view, FOV)180~240 mm2。管电压120 kV,开启DoseRight管电流调制模式,DoseRight Index 28;探测器64×0.625 mm;螺距0.984;转速0.5 s/r。
1.2.2 图像重建与重组
重建区域包全腰椎内固定假体,分别使用FBP和不同等级iDose4对骨算法(等级1~7)及软组织算法(等级1~6)进行离线重建,同时重建使用和不使用O-MAR的图像。骨算法滤过函数Y-Sharp(YA),窗宽
2000 HU,窗位200 HU;软组织算法滤过函数Standard(B),窗宽350 HU,窗位40 HU。层厚1 mm,层间距1 mm,FOV 200 mm2,矩阵512×512。图像重组。使用软件包CT Viewer的比较(compare)模式,并开启关联(link),保证重组每个病例的所有序列的层面绝对一致,层厚1 mm。骨算法重组螺钉显示最佳的横断面和矢状面图像;软组织算法重组螺钉显示最佳和螺钉区域内椎间盘正中层面的横断面图像。
1.3 图像质量评价
1.3.1 客观评价
在显示螺钉长轴最佳的横断图像上画圆形感兴趣区a(图1)作为信号区,面积50~55 mm2,骨算法图像放置于植入物旁椎体的骨质中间,软组织算法图像放置于植入物附近受影响较严重的肌肉,注意避开钢钉。在匀质海绵区画感兴趣区b(面积同a)作为背景区,分别记录CT值的标准差 SDa和SDb。SDb代表感兴趣区噪声水平。
所有感兴趣区均测量2次取平均值。计算伪影指数(artifact index, AI)[6-8]:
$$ \mathrm{AI}=\sqrt{\mathrm{S}\mathrm{D}_{\mathrm{a}}^2-\mathrm{S}\mathrm{D}_{\mathrm{b}}^2}\;。 $$ (1) 1.3.2 主观评价
由两名经验丰富的放射科医师采用双盲法完成图像质量评分。对骨算法和软组织算法FBP及不同等级iDose4图像进行使用O-MAR前后的金属伪影和诊断信息两方面分别评分。
采用3分制。①金属伪影抑制情况:1分,植入物旁金属伪影重,周围组织结构显示欠佳;2分,植入物旁金属伪影较少,周围组织结构显示较清晰;3分,植入物旁金属伪影基本去除,周围组织结构显示清晰。②骨算法诊断信息:1分,植入物毗邻的骨皮质、骨小梁等细节显示欠佳,诊断信息丢失较多;2分,植入物毗邻的骨皮质、骨小梁等细节显示尚可,诊断信息有一定丢失;3分,植入物毗邻的骨皮质、骨小梁等细节显示较好,诊断信息丢失较少或没有丢失。③软组织算法诊断信息:1分,植入物毗邻的椎间盘、椎管及邻近组织显示欠佳,诊断信息丢失较多;2分,植入物毗邻的椎间盘、椎管及邻近组织显示尚可,诊断信息有一定丢失;3分,植入物毗邻的椎间盘、椎管及邻近组织显示较好,诊断信息丢失较少或没有丢失。
1.4 统计学分析
采用SPSS 21.0统计分析软件。计量资料满足正态分布和方差齐性时以
$ \left(\overline{x}\pm s\right) $ 表示,不满足的计量资料和主观评分以中位数和四分位数间距表示。客观评价。使用O-MAR前后SD和AI的比较,骨算法采用配对t检验,软组织算法采用Wilcoxon配对秩和检验;FBP及不同等级iDose4比较,骨算法采用独立样本秩和检验,软组织算法采用单因素方差分析,P < 0.05为差异有统计学意义。当总体差异有统计学意义时进行两两比较,采用Bonferroni校正后的显著性水平[9]。
主观评价。Kappa检验评价两位医师评分一致性,Kappa > 0.6为一致性好。使用O-MAR前后图像评分采用Wilcoxon配对秩和检验,FBP及不同等级iDose4的比较采用多个独立样本秩和检验。
2. 结果
2.1 客观评价
2.1.1 使用/不使用O-MAR
FBP或任一等级iDose4的骨和软组织算法图像使用O-MAR时,SD值和AI值均低于不使用O-MAR的图像,差异有显著统计学意义(表1)。
表 1 使用/不使用O-MAR的图像SD值、AI值比较Table 1. Comparison of SD and AI values of images with/without O-MAR重建算法 评价指标 骨算法 统计检验 软组织算法 统计检验 不使用O-MAR 使用O-MAR t P 不使用O-MAR 使用O-MAR Z P FBP SD 372.93±95.17 336.37±89.86 10.059 < 0.001 61.65
(49.75,76.88)45.90
(38.48,50.80)−3.920 < 0.001 AI 364.55±95.95 327.23±90.88 9.939 59.37
(46.22,70.46)40.64
(31.65,46.43)−3.920 iDose4-1 SD 335.27±85.25 301.74±80.54 9.103 < 0.001 54.10
(45.38,70.98)40.05
(35.60,46.78)−3.920 < 0.001 AI 327.52±85.81 292.91±81.49 9.066 51.59
(42.21,61.82)35.45
(28.78,42.47)−3.920 iDose4-2 SD 314.66±79.66 282.22±75.32 8.157 < 0.001 50.45
(43.20,66.65)37.75
(33.45,44.53)−3.921 < 0.001 AI 307.26±80.20 273.72±76.22 8.157 48.05
(40.18,58.50)32.24
(27.19,39.86)−3.920 iDose4-3 SD 293.10±73.82 262.18±69.79 7.628 < 0.001 46.75
(40.73,62.08)34.85
(30.88,42.28)−3.920 < 0.001 AI 286.09±74.37 254.07±70.66 7.598 44.22
(37.72,55.54)29.84
(25.23,37.15)−3.920 iDose4-4 SD 268.78±67.41 239.97±63.74 6.880 < 0.001 43.40
(37.75,56.75)31.60
(27.58,39.60)−3.920 < 0.001 AI 262.19±67.91 232.25±64.56 6.904 40.94
(36.03,48.62)27.64
(22.87,33.97)−3.920 iDose4-5 SD 243.36±60.97 215.43±57.18 5.884 < 0.001 40.10
(33.55,50.18)28.65
(23.15,35.65)−3.920 < 0.001 AI 237.27±61.49 208.16±57.94 5.932 37.62
(31.65,43.21)25.66
(19.23,30.09)−3.920 iDose4-6 SD 214.33±53.84 187.84±49.78 5.002 < 0.001 36.95
(31.20,43.88)26.90
(20.43,31.85)−3.920 < 0.001 AI 208.82±54.36 181.09±50.49 5.075 33.71
(29.73,39.55)22.17
(16.32,26,54)−3.920 iDose4-7 SD 180.81±46.48 155.63±41.40 4.139 < 0.001 AI 176.04±47.03 149.52±42.04 4.234 2.1.2 使用FBP及不同迭代等级iDose4 O-MAR图像
(1)骨算法。iDose4各等级图像AI值均低于FBP,其中iDose4-5~7 与FBP差异有统计学意义。
不同等级iDose4图像的AI值随等级升高而逐渐降低,其中:iDose4-1与iDose4-5~7、iDose4-2与iDose4-6~7、iDose4-3~4与iDose4-7图像的AI值有统计学差异,其余等级间两两比较均不存在统计学差异。
(2)软组织算法。iDose4各等级图像AI值均低于FBP,其中iDose4-3~6 与FBP差异有统计学意义。不同等级iDose4图像的AI值随等级升高而逐渐降低,其中:iDose4-1与iDose4-5~6、iDose4-2~3与iDose4-6图像的AI值有统计学差异,其余等级间两两比较均不存在统计学差异。
2.2 主观评价
两名医师的图像评分的一致性好(Kappa值在0.6~0.8之间)。
2.2.1 使用/不使用O-MAR
(1)骨算法。使用O-MAR的图像金属伪影和诊断信息评分高于不使用的图像,差异具有统计学意义(表2)。使用O-MAR图像较不使用O-MAR图像金属伪影少、图像质量好(图2)。
表 2 骨算法评分值Table 2. Score of bone algorithm金属伪影 诊断信息 医师1 医师2 医师1 医师2 算法 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR FBP 2(2,2) 1(1,1) 2(2,2) 1(1,1) 2(2,2) 1(1,1) 2(2,2) 1(1,1) iDose4-1 2(2,2) 1(1,1) 2(2,2) 1(1,1) 2(2,2) 1(1,1) 2(2,2) 1(1,1) iDose4-2 2(2,2) 1(1,1) 2(2,2) 1(1,1) 3(2,3) 1(1,1) 3(2,3) 1(1,1) iDose4-3 2(2,2) 1(1,1) 2(2,3) 1(1,1) 3(3,3) 1(1,1) 3(3,3) 1(1,1) iDose4-4 2(2,3) 1(1,1) 2(2,3) 1(1,1) 3(2,3) 1(1,1) 2(2.25,3) 1(1,1) iDose4-5 3(3,3) 1(1,2) 3(3,3) 1(1,2) 2(2,2) 1(1,1.75) 2(2,3) 1(1,2) iDose4-6 3(3,3) 2(1,2) 3(3,3) 2(1,2) 2(2,2) 1(1,2) 2(2,2) 1(1,2) iDose4-7 3(3,3) 2(1,2) 3(2.25,3) 2(1,2) 2(2,2) 1(1,1) 2(2,2) 1.5(1,2) Z −11.318 −11.208 −10.662 −10.008 P < 0.001 < 0.001 < 0.001 < 0.001 (2)软组织算法。使用O-MAR的图像金属伪影被良好抑制,评分高于不使用的;但使用O-MAR导致新伪影的出现,不使用O-MAR的图像诊断信息评分高于使用的,差异有统计学意义(表3和图3)。
表 3 软组织算法评分值Table 3. Score of soft tissue algorithm金属伪影 诊断信息 医师1 医师2 医师1 医师2 算法 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR FBP 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(2,2) 2(1,2) 2(2,2) iDose4-1 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(2,2) 2(1,2) 2(2,2) iDose4-2 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(2,2) 2(1,2) 2(2,2) iDose4-3 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(2,2) 2(1,2) 2(2,2) iDose4-4 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(1.25,2) 2(1,2) 2(2,2) iDose4-5 2(2,2) 1.5(1,2) 2(2,2) 1.5(1,2) 1(1,2) 1(1,2) 1(1,2) 2(1.25,2) iDose4-6 2(2,2) 2(1,2.75) 2(2,2) 2(1,2) 1(1,1) 1(1,1) 1(1,1.75) 2(1,2) Z −7.233 −6.794 4.989 6.057 P < 0.001 < 0.001 < 0.001 < 0.001 2.2.2 使用FBP及不同等级iDose4
(1)骨算法O-MAR图像。FBP及iDose4-1~7等级金属伪影和诊断信息评分均存在统计学差异。金属伪影方面:两名医师评分结果iDose4-5~7高于FBP和iDose4-1~2,医师1还认为iDose4-3低于iDose4-5~7,iDose4-4低于iDose4-6~7。诊断信息方面:两名医师评分结果iDose4-2~4高于FBP,iDose4-3评分最高(图4)。
(2)软组织算法(使用O-MAR和不使用O-MAR图像)。无论使用或不使用 O-MAR,图像评分统计结果相同:对金属伪影,两名医师评分结果显示整体不存在差异;对诊断信息,医师1结果显示FBP及iDose4-1~4分别与iDose4-6存在统计学差异。而医师2结果整体无差异。
3. 讨论
腰椎内固定手术的术后评估不仅需要观察相关区域骨质情况,还需要观察椎间盘是否有压迫,椎管有无狭窄以及植入物附近有无气体、出血等。故扫描后重建算法和参数的合理选择尤为重要。
本研究重建了骨和软组织两种算法的原始图像,在此基础上分两部分讨论:第1部分对比使用O-MAR前后图像噪声、伪影以及诊断信息的差异;第2部分探讨应用FBP及不同迭代等级金属伪影和诊断信息的差异。综合分析,旨在量化O-MAR和迭代算法对提高图像质量的作用,并找到能够最大程度减少金属伪影,同时又能够提供较好诊断学信息的参数组合,为临床诊疗和术后评估提供可靠的影像学依据。
O-MAR技术现已广泛应用于临床,它对图像的迭代重建只针对金属像素,不会影响图像中其他像素的显示[10-11]。据文献报道,O-MAR还可用于减少高浓度造影剂[12]、颅内动脉瘤栓塞术后[13]等产生机制与金属相似的伪影;iDose4是新一代迭代重建技术,相比于传统FBP能够降低图像噪声[14],提高可视化图像分辨率,级别越高,能力越强[15]。但iDose4重建的运算量可达FBP的100倍以上,等级越高运算量越大,影响工作效率[16]。
本研究中,骨算法图像使用O-MAR重建,噪声和伪影指数均显著降低,观察者对伪影抑制效果和诊断信息的评分显著提高,螺钉上下和前方低密度金属伪影面积明显减小,邻近骨质无明显缺失,基本无诊断信息丢失,证明对FBP及所有迭代等级,O-MAR都能够很好地起到降低图像噪声、减少金属伪影、改善图像质量的作用。该结果与既往一些研究结论一致[1,17-19]。但也有研究持相反观点[20],认为对于骶髂关节融合术后图像,不使用O-MAR的整体图像质量、骶骨和植入物显示均优于使用O-MAR的图像,不推荐使用O-MAR进行这类患者的随访。
不同等级iDose4图像质量评价结果表明,迭代等级增高,图像噪声减小,伪影指数下降;针对金属伪影抑制效果的主观评分结果显示,iDose4-5~7等级的图像相对于中低迭代等级的图像伪影抑制效果更佳。诊断信息的主观评分结果显示,中等级别iDose4-2~4的图像评分较高,iDose4-3评分最高。这是因为随着迭代等级的增高,图像过度平滑,锐利度降低(图4)。骨算法图像的重要观察要点是骨皮质、骨小梁等结构的显示,FBP和低迭代iDose4-1图像颗粒感较重,骨质显示较粗糙;高迭代iDose4-5~7图像过于平滑,有失真感,整体视觉效果和骨皮质、骨小梁的显示不佳。而中间迭代iDose4-2~4图像的颗粒感与平滑程度适中,各诊断要点信息显示最好。以上表现与张青帝等[21]对冠状动脉CT的研究所见一致。
综上,iDose4-5~7虽然噪声最低,去金属伪影效果最好,但其在诊断信息的评分上明显低于iDose4-2~4。本研究认为O-MAR联合iDose4-2~4使用,影像质量较优,并以O-MAR联合使用iDose4-3等级时为最优。
软组织算法使用或不使用O-MAR的图像客观指标的差别同骨算法,O-MAR对于螺钉层面金属伪影的减少和图像质量的改善效果显著。
椎间盘层面横断面图像不使用O-MAR时,金属伪影存在于植入物附近,呈向四周密集放射的细条状低密度(图3 (a)),影响植入物周围肌肉的显示;而使用O-MAR的图像金属伪影虽然被抑制,但会出现分布在其他位置(椎间盘等)的新伪影,呈分散放射的粗条状(图3 (b))。这类伪影的产生机制可能是数据分割不准确[22],一定程度上去除了图像信息。这一点在主观评分中得以充分体现:对于金属伪影,使用O-MAR的图像植入物附近金属伪影的抑制效果显著。而对诊断信息,两名观察者都认为不使用O-MAR重建的图像整体评分较高。这是因为不使用O-MAR,虽然周围组织显示欠佳,但椎间盘和椎管的显示较好,而使用O-MAR的图像恰好相反,使用O-MAR对植入物周围组织的显示效果有所提升,但会影响椎间盘和椎管的显示。综合分析,不使用O-MAR的图像评分略高。一项关于颅内金属植入物CT血管造影的研究呈现了类似结果[23]:68.1%的O-MAR图像产生了新的条纹伪影。
众所周知,每一个观察要点对影像诊断的精准性都有意义,故以上结论不能代表软组织算法不使用O-MAR的图像可代替使用O-MAR的图像,相反,两种重建算法应结合使用。
软组织算法应用不同等级iDose4,客观指标变化趋势与骨算法相同。主观评分无论是否使用O-MAR,不同迭代等级对伪影都没有影响。对诊断信息,医师2认为不同迭代等级之间没有差异,医师1也仅认为高迭代iDose4-6的分数相较于其他等级略低。故迭代算法对有严重金属伪影的软组织算法图像而言意义不大。
综上所述,建议联合使用O-MAR技术和中间迭代等级iDose4-3重建骨算法图像;重建软组织算法图像时不推荐使用迭代算法,建议同时重建O-MAR和不使用O-MAR的图像以便配合观察。
本研究不足之处:①本研究样本量较少;②本研究未考虑不同病例间植入物位置不完全相同的影响;③未考虑不同植入物材料所产生的影响,未来的研究可按植入物材料分类,探究不同材料是否会影响参数选择,进而提出针对每种材料的检查方案。
-
表 1 使用/不使用O-MAR的图像SD值、AI值比较
Table 1 Comparison of SD and AI values of images with/without O-MAR
重建算法 评价指标 骨算法 统计检验 软组织算法 统计检验 不使用O-MAR 使用O-MAR t P 不使用O-MAR 使用O-MAR Z P FBP SD 372.93±95.17 336.37±89.86 10.059 < 0.001 61.65
(49.75,76.88)45.90
(38.48,50.80)−3.920 < 0.001 AI 364.55±95.95 327.23±90.88 9.939 59.37
(46.22,70.46)40.64
(31.65,46.43)−3.920 iDose4-1 SD 335.27±85.25 301.74±80.54 9.103 < 0.001 54.10
(45.38,70.98)40.05
(35.60,46.78)−3.920 < 0.001 AI 327.52±85.81 292.91±81.49 9.066 51.59
(42.21,61.82)35.45
(28.78,42.47)−3.920 iDose4-2 SD 314.66±79.66 282.22±75.32 8.157 < 0.001 50.45
(43.20,66.65)37.75
(33.45,44.53)−3.921 < 0.001 AI 307.26±80.20 273.72±76.22 8.157 48.05
(40.18,58.50)32.24
(27.19,39.86)−3.920 iDose4-3 SD 293.10±73.82 262.18±69.79 7.628 < 0.001 46.75
(40.73,62.08)34.85
(30.88,42.28)−3.920 < 0.001 AI 286.09±74.37 254.07±70.66 7.598 44.22
(37.72,55.54)29.84
(25.23,37.15)−3.920 iDose4-4 SD 268.78±67.41 239.97±63.74 6.880 < 0.001 43.40
(37.75,56.75)31.60
(27.58,39.60)−3.920 < 0.001 AI 262.19±67.91 232.25±64.56 6.904 40.94
(36.03,48.62)27.64
(22.87,33.97)−3.920 iDose4-5 SD 243.36±60.97 215.43±57.18 5.884 < 0.001 40.10
(33.55,50.18)28.65
(23.15,35.65)−3.920 < 0.001 AI 237.27±61.49 208.16±57.94 5.932 37.62
(31.65,43.21)25.66
(19.23,30.09)−3.920 iDose4-6 SD 214.33±53.84 187.84±49.78 5.002 < 0.001 36.95
(31.20,43.88)26.90
(20.43,31.85)−3.920 < 0.001 AI 208.82±54.36 181.09±50.49 5.075 33.71
(29.73,39.55)22.17
(16.32,26,54)−3.920 iDose4-7 SD 180.81±46.48 155.63±41.40 4.139 < 0.001 AI 176.04±47.03 149.52±42.04 4.234 表 2 骨算法评分值
Table 2 Score of bone algorithm
金属伪影 诊断信息 医师1 医师2 医师1 医师2 算法 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR FBP 2(2,2) 1(1,1) 2(2,2) 1(1,1) 2(2,2) 1(1,1) 2(2,2) 1(1,1) iDose4-1 2(2,2) 1(1,1) 2(2,2) 1(1,1) 2(2,2) 1(1,1) 2(2,2) 1(1,1) iDose4-2 2(2,2) 1(1,1) 2(2,2) 1(1,1) 3(2,3) 1(1,1) 3(2,3) 1(1,1) iDose4-3 2(2,2) 1(1,1) 2(2,3) 1(1,1) 3(3,3) 1(1,1) 3(3,3) 1(1,1) iDose4-4 2(2,3) 1(1,1) 2(2,3) 1(1,1) 3(2,3) 1(1,1) 2(2.25,3) 1(1,1) iDose4-5 3(3,3) 1(1,2) 3(3,3) 1(1,2) 2(2,2) 1(1,1.75) 2(2,3) 1(1,2) iDose4-6 3(3,3) 2(1,2) 3(3,3) 2(1,2) 2(2,2) 1(1,2) 2(2,2) 1(1,2) iDose4-7 3(3,3) 2(1,2) 3(2.25,3) 2(1,2) 2(2,2) 1(1,1) 2(2,2) 1.5(1,2) Z −11.318 −11.208 −10.662 −10.008 P < 0.001 < 0.001 < 0.001 < 0.001 表 3 软组织算法评分值
Table 3 Score of soft tissue algorithm
金属伪影 诊断信息 医师1 医师2 医师1 医师2 算法 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR 使用O-MAR 不使用O-MAR FBP 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(2,2) 2(1,2) 2(2,2) iDose4-1 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(2,2) 2(1,2) 2(2,2) iDose4-2 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(2,2) 2(1,2) 2(2,2) iDose4-3 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(2,2) 2(1,2) 2(2,2) iDose4-4 2(2,2) 1(1,2) 2(2,2) 1(1,2) 2(1,2) 2(1.25,2) 2(1,2) 2(2,2) iDose4-5 2(2,2) 1.5(1,2) 2(2,2) 1.5(1,2) 1(1,2) 1(1,2) 1(1,2) 2(1.25,2) iDose4-6 2(2,2) 2(1,2.75) 2(2,2) 2(1,2) 1(1,1) 1(1,1) 1(1,1.75) 2(1,2) Z −7.233 −6.794 4.989 6.057 P < 0.001 < 0.001 < 0.001 < 0.001 -
[1] 房加高, 邹月芬, 徐海, 等. O-MAR技术在去除腰椎金属植入物伪影中的应用价值[J]. 海南医学, 2018, 29(10): 1408-1410. DOI: 10.3969/j.issn.1003-6350.2018.10.023. FANG J G, ZOU Y F, XU H, et al. Value of O-MAR iterative algorithm in removing metal artifacts of lumbar implants[J]. Hainan Medical Journal, 2018, 29(10): 1408-1410. DOI: 10.3969/j.issn.1003-6350.2018.10.023. (in Chinese).
[2] CHOO H J, LEE S J, KIM D W, et al. Comparison of the quality of various polychromatic and monochromatic dual-energy CT images with or without a metal Artifact reduction algorithm to evaluate total knee arthroplasty[J]. Korean Journal of Radiology, 2021, 22(8): 1341-1351. DOI: 10.3348/kjr.2020.0548.
[3] 王平, 高玉颖, 卢再鸣, 等. 迭代重组IMR技术和iDose4技术在腹部低剂量CT扫描乏血供肝转移瘤中的图像质量[J]. 中华放射学杂志, 2015, 49(4): 283-287. DOI: 10.3760/cma.j.issn.1005-1201.2015.04.011. WANG P, GAO Y Y, LU Z M, et al. Iterative model reconstruction and hybrid iterative reconstruction techniques iDose4 in low-dose abdominal CT: Comparison of image quality in evaluation of hypovascular metastases of liver[J]. Chinese Journal of Radiology, 2015, 49(4): 283-287. DOI: 10.3760/cma.j.issn.1005-1201.2015.04.011. (in Chinese).
[4] CHO Y J, SCHOEPF U J, SILVERMAN J R, et al. Iterative image reconstruction techniques: Cardiothoracic computed tomography applications[J]. Journal of Thoracic Imaging, 2014, 29(4): 198-208. DOI: 10.1097/RTI.0000000000000041.
[5] 侯阳, 于兵, 郭启勇, 等. 迭代重建对前置门控冠状动脉CT图像质量及辐射剂量的影响[J]. 中华放射学杂志, 2013, 47(4): 305-309. DOI: 10.3760/cma.j.issn.1005-1201.2013.04.004. HOU Y, YU B, GUO Q Y, et al. Application of iterative reconstruction in prospective electrocardiography-triggered CT coronary angiography[J]. Chinese Journal of Radiology, 2013, 47(4): 305-309. DOI: 10.3760/cma.j.issn.1005-1201.2013.04.004. (in Chinese).
[6] 李杰, 袁源, 王春杰, 等. 能谱CT去金属伪影(MAR)技术用于减低单髋关节置换物伪影[J]. 中国医学影像技术, 2021, 37(1): 131-135. DOI: 10.13929/j.issn.1003-3289.2021.01.032. LI J, YUAN Y, WANG C J, et al. Energy spectrum CT metal artifacts reduction (MAR) for reducing artifacts of unilateral hip arthroplasty[J]. Chinese Journal of Medical Imaging Technology, 2021, 37(1): 131-135. DOI: 10.13929/j.issn.1003-3289.2021.01.032. (in Chinese).
[7] HU Y, PAN S, ZHAO X, et al. Value and clinical application of orthopedic metal artifact reduction algorithm in CT scans after orthopedic metal implantation[J]. Korean Journal of Radiology, 2017, 18(3): 526-535. DOI: 10.3348/kjr.2017.18.3.526.
[8] GROßE H N, NEUHAUS V, ABDULLAYEV N, et al. Reduction of artifacts caused by orthopedic hardware in the spine in spectral detector CT examinations using virtual monoenergetic image reconstructions and metal-artifact-reduction algorithms[J]. Skeletal Radiology, 2018, 47(2): 195-201. DOI: 10.1007/s00256-017-2776-5.
[9] 刘丹丹, 崔莹, 赵波, 等. 定位像扫描参数对胸部CT影像质量和辐射剂量影响的模体研究[J]. 中华放射医学与防护杂志, 2021, 41(3): 217-221. DOI: 10.3760/cma.j.issn.0254-5098.2021.03.011. LIU D D, CUI Y, ZHAO B, et al. The influence of scout scanning parameters on image quality and radiation dose of chest CT: A phantom study[J]. Chinese Journal of Radiological Medicine and Protection, 2021, 41(3): 217-221. DOI: 10.3760/cma.j.issn.0254-5098.2021.03.011. (in Chinese).
[10] 李晓莉, 冯卫华, 董诚, 等. CT能谱成像技术减除金属植入物伪影的定量实验研究[J]. 中华放射学杂志, 2011, 45(8): 736-739. DOI: 10.3760/cma.j.issn.1005-1201.2011.08.007. LI X L, FENG W H, DONG C, et al. The experimental quantitative study of spectral CT imaging in reducing the metal artifacts[J]. Chinese Journal of Radiology, 2011, 45(8): 736-739. DOI: 10.3760/cma.j.issn.1005-1201.2011.08.007. (in Chinese).
[11] HILGERS G, NUVER T, MINKEN A. The CT number accuracy of a novel commercial metal artifact reduction algorithm for large orthopedic implants[J]. Journal of Applied Clinical Medical Physics, 2014, 15(1): 4597. DOI: 10.1120/jacmp.v15i1.4597.
[12] 吴志斌, 李剑, 郑敏文, 等. O-MAR技术在减少高浓度造影剂硬化伪影中的应用价值[J]. 中国医疗设备, 2019, 34(6): 9-11. DOI: 10.3969/j.issn.1674-1633.2019.06.003. WU Z B, LI J, ZHENG M W, et al. Application of O-MAR technology in reducing the artifacts of high concentration contrast medium[J]. China Medical Devices, 2019, 34(6): 9-11. DOI: 10.3969/j.issn.1674-1633.2019.06.003. (in Chinese).
[13] 宋殿行, 郭鹏, 王玉琦, 等. O-MAR重组在减少颅内动脉瘤弹簧圈栓塞术后金属伪影的价值[J]. 临床放射学杂志, 2020, 39(3): 592-595. DOI: 10.13437/j.cnki.jcr.2020.03.037. SONG D X, GUO P, WANG Y Q, et al. Clinical evaluation of orthopedic metal artifact reduction (O-MAR) in reducing metallic artifacts in CT of intracranial aneurysms after endovascular coil treatment[J]. Journal of Clinical Radiology, 2020, 39(3): 592-595. DOI: 10.13437/j.cnki.jcr.2020.03.037. (in Chinese).
[14] 王茹, 姜彦, 徐凯, 等. iDose4与O-MAR迭代算法对TACE术后CT成像质量和疗效评估的价值[J]. 中国医学计算机成像杂志, 2016, 22(5): 457-462. DOI: 10.3969/j.issn.1006-5741.2016.05.014. WANG R, JIANG Y, XU K, et al. Effect of iDose4 and O-MAR iterative algorithm on imaging quality of CT scan after TACE operation[J]. Chinese Computed Medical Imaging, 2016, 22(5): 457-462. DOI: 10.3969/j.issn.1006-5741.2016.05.014. (in Chinese).
[15] 袁肖娜, 高知玲, 朱凯, 等. iDose迭代重建算法对上腹部CT图像质量的影响[J]. 实用放射学杂志, 2016, 32(1): 102-106. DOI: 10.3969/j.issn.1002-1671.2016.01.027. YUAN X N, GAO Z L, ZHU K, et al. The effect of iDose iterative reconstruction algorithm on the image quality of upper abdomen CT scan[J]. Journal of Practical Radiology, 2016, 32(1): 102-106. DOI: 10.3969/j.issn.1002-1671.2016.01.027. (in Chinese).
[16] JOEMAI R M, GELEIJINS J, VELDKAMP W J. Development and validation of a low dose simulator for computed tomography[J]. European Radiology, 2010, 20(4): 958-966. DOI: 10.1007/s00330-009-1617-x.
[17] NEUHAUS V, GROSSE H N, ZOPFS D, et al. Reducing artifacts from total hip replacements in dual layer detector CT: Combination of virtual monoenergetic images and orthopedic metal artifact reduction[J]. European Journal of Radiology, 2019, 111: 14-20. DOI: 10.1016/j.ejrad.2018.12.008.
[18] AKDENIZ Y, YEGINGIL I, YEGINGIL Z. Effects of metal implants and a metal artifact reduction tool on calculation accuracy of AAA and acuros XB algorithms in small fields[J]. Medical Physics, 2019, 46(11): 5326-5335. DOI: 10.1002/mp.13819.
[19] 李杰, 孙兴文, 欧阳汉强, 等. 能谱CT去金属伪影技术减低脊柱不同类型植入物伪影的体模研究[J]. 中华放射学杂志, 2021, 55(9): 910-916. DOI: 10.3760/cma.j.cn112149-20200914-01086. LI J, SUN X W, OUYANG H Q, et al. The experimental phantom study of spectral CT metal artifact reduction technique in reducing the artifacts of different types of spinal implants[J]. Chinese Journal of Radiology, 2021, 55(9): 910-916. DOI: 10.3760/cma.j.cn112149-20200914-01086. (in Chinese).
[20] SELLES M, KORTE J H, BOELHOUWERS H J, et al. Metal artifact reduction in computed tomography: Is it of benefit in evaluating sacroiliac joint fusion?[J]. European Journal of Radiology, 2022, 148: 110159. DOI: 10.1016/j.ejrad.2022.110159.
[21] 张青帝, 吴丽卓, 姜晓静, 等. 不同级别iDose4迭代重建技术在冠状动脉CT成像中的应用[J]. 中国实验诊断学, 2016, 20(5): 752-754. ZHANG Q D, WU L Z, JIANG X J, et al. Application of different level iDose4 iterative reconstruction technique in coronary computed tomography angiography[J]. Chinese Journal of Laboratory Diagnosis, 2016, 20(5): 752-754. (in Chinese).
[22] BARRETO I, PEPIN E, DAVIS I, et al. Comparison of metal artifact reduction using single-energy CT and dual-energy CT with various metallic implants in cadavers[J]. European Journal of Radiology, 2020, 133: 109357. DOI: 10.1016/j.ejrad.2020.109357.
[23] SUNWOO L, PARK S W, RHIM J H, et al. Metal artifact reduction for orthopedic implants: Brain CT angiography in patients with intracranial metallic implants[J]. Journal of Korean Medical Science, 2018, 33(21): e158. DOI: 10.3346/jkms.2018.33.e158.




 下载:
下载: