Preliminary exploration of non-gated high-pitch chest CT combined with artificial intelligence in assessing coronary artery calcium score
-
摘要:
目的:探讨非门控大螺距肺CT联合人工智能技术对冠脉钙化积分测量的可行性。方法:回顾性分析24例同时接受非门控大螺距肺CT和冠状动脉钙化积分CT扫描的患者图像。两个扫描组参数设置:①非门控大螺距肺CT平扫:CarekV和CareDose 4D,ref.kV 110,ref.mAs 80,螺距3,滤过核BR40。②心电门控冠状动脉钙化积分CT:CarekV,CareDose 4D,ref.kV 120,ref.mAs 50,螺距0.15,采集R-R间期35%以及75%,滤过核QR36。两组图像窗宽/窗位345/50,层厚/间隔3 mm/1.5 mm。两个扫描组图像根据3种测量方法(Syngo.via工作站测量、AI测量、AI+手动校正测量)各分为三个亚组,进行钙化积分(Agatston Score,AS)测量和风险分级,并记录工作站测量以及AI+手动校正测量所用时间。记录两种检查容积剂量指数(CTDIvol)、剂量长度乘积(DLP),并计算有效剂量(ED)。使用SPSS Statistics 27.0软件进行统计分析。结果:①大螺距肺CT管电压分别为100、110、120 kV,冠状动脉钙化积分CT均为120 kV。②大螺距肺CT和冠状动脉钙化积分CT的ED分别为(2.1±0.4)、(2.1±0.7) mSv。③大螺距肺CT的3种测量方法所得AS有统计学差异(X2=27.163,P<0.001),但AS一致性较高(ICC:0.988)。④大螺距肺CT联合AI(X2=4.795,P=0.091、ICC:0.990)、大螺距肺CT工作站(Z=0.912,P=0.362、ICC:0.988)、门控钙化积分联合AI(X2=10.900,P=0.004、ICC:0.980)分别与冠脉钙化积分工作站测得AS,均无统计学差异且一致性较高。⑤AI所得风险分级一致性很强,加权Kappa系数均在0.818-1.000之间。⑥两个扫描组的工作站与AI+手动校正测量所用时间均有统计学差异(Z =4.200、4.049,均P<0.001)。结论:非门控大螺距肺CT联合AI可获得可靠的冠脉钙化积分和风险分级结果且耗时短,具有较好的临床应用价值。
Abstract:Objective: To investigate the feasibility of using non-gated high-pitch chest computed tomography (CT) combined with artificial intelligence (AI) technology to measure the coronary artery calcium score. Methods: In this retrospective analysis, we reviewed the images of 24 patients who underwent both non-gated high-pitch chest CT and coronary artery calcium scoring CT. The scanning parameters were as follows: ① non-gated high-pitch chest CT scan: CarekV and CareDose 4D, ref.kV 110, ref.mAs 80, pitch 3, filter core BR40; ② ECG-gated coronary artery calcification score CT: CarekV, CareDose 4D, ref.kV 120, ref.mAs 50, pitch 0.15, acquisition R-R interval 35% and 75%, filter core QR36. The image window width/window level of the two groups was 345/50, and the slice thickness/interval was 3 mm/1.5 mm. The images of the two scan groups were divided into three subgroups according to the three measurement methods (Syngo.via workstation measurement, AI measurement, and AI + manual correction measurement). The image calcification score (Agatston Score, AS) was measured, risk classification was performed, and the time taken for the workstation measurement and the AI + manual correction measurement was recorded. The volume dose index (CTDIvol) and dose-length product (DLP) of the two examinations were recorded, and the effective dose (ED) was calculated. SPSS Statistics software (version 27.0) was used for the statistical analysis. Results: The tube voltages of the high-pitch chest CT were 100, 110, and 120 kV, and the coronary artery calcium score was 120 kV. EDs of high-pitch chest CT and coronary artery calcium score CT were 2.1±0.4 and 2.1±0.7 mSv, respectively. The three measurement methods used for high-pitch chest CT showed significant differences in AS (X2=27.163, P < 0.001), but the consistency of AS was high (ICC: 0.988). Regarding AS measurement, high-pitch chest CT combined with AI (X2 = 4.795, P = 0.091, ICC: 0.990), high-pitch chest CT using a workstation (Z = 0.912, P = 0.362, ICC: 0.988), and gated calcium scoring combined with AI (X2 = 10.900, P = 0.004, ICC: 0.980) showed no significant differences or high consistency compared to the workstation for coronary artery calcium scoring. The risk classification obtained by the AI was highly consistent, and the weighted kappa coefficients were between 0.818 and 1.000. The time taken for measurements using the workstation and AI + manual correction in both scanning groups showed significant differences (Z = 4.200, 4.049, P < 0.001). Conclusion: Non-gated high-pitch chest CT combined with AI can provide reliable results for artery calcium scores and risk classification with reduced time consumption, demonstrating substantial clinical utility.
-
Keywords:
- calcium Score /
- large pitch /
- chest CT /
- artificial intelligence
-
近年来,人工智能(AI)技术在医学影像分析领域快速发展,在一份调查报告中显示,AI用于冠状动脉分析的普及率已从2019年占比6%迅速提高到了58%[1]。其中AI结合非门控肺CT扫描分析冠状动脉钙化已然成为了一个新兴研究方向[2−3],尤其是低剂量肺CT具有冠状动脉钙化检测和分级的潜力[4],并且表现出了可靠的重复性[5]。这种方法是在无心电门控监测下,利用常规肺部CT扫描结合AI测量钙化积分,从而大大提高了临床效率,并且为扩大筛查范围提供了重要保证。但是由于AI测量的准确性受到输入图像质量的影响[6],且常规肺部CT检查,扫描时间较长,往往存在心脏搏动伪影,这会影响冠状动脉的清晰度和AI测量钙化积分的准确性。因此,本研究探讨非门控大螺距肺CT联合AI技术,是否可以提高冠脉钙化积分的准确性以及在临床实践中的可行性。
1. 材料与方法
1.1 实验材料
Simens双源Force CT机(德国Simens公司);Simens Syngo.via工作站;联影AI门控钙化积分测量模块、联影AI非门控钙化积分测量模块。
1.2 一般资料
回顾性选取2022年7月至2022年11月,在我院同时进行非门控大螺距肺CT平扫和心电门控冠状动脉钙化积分CT扫描的患者30例。入组标准:未进行心脏搭桥手术;未安装心脏起搏器;未放置冠状动脉支架。排除标准:心电门控冠状动脉钙化积分为0;图像存在严重伪影影响诊断。最终纳入24例患者,平均年龄33 ~ 84(60.32±12.34)岁。男16例,女8例。BMI:20.4 ~ 38(25.98±3.74),心率46 ~ 97(66.42±10.96)次/分。
本研究获医学伦理委员会批准,伦理号为TREC2022-KY035。
1.3 扫描参数设置
1.3.1 非门控大螺距肺CT平扫参数
定位像:X射线投照角度选择0°(即前后位定位像),管电压120 kV,管电流20 mA。正式扫描:自动管电压调制技术(CarekV)和自动管电流调制技术(CareDose 4 D),参考管电压110 kV,参考管电流80 mAs,探测器宽度192×0.6 mm,旋转时间0.25 s,螺距3。
1.3.2 心电门控冠状动脉钙化积分CT参数
定位像扫描同上。正式扫描:CarekV,CareDose 4 D,参考管电压120 kV,参考管电流50 mAs,螺距0.15。采集R-R间期35%以及75%,选择冠状动脉显示好,伪影小的时相。其余参数与非门控大螺距肺CT扫描参数一致。
1.4 图像重组
两种扫描方式均重组心脏范围的轴位图像。滤过核:大螺距肺CT为BR40;冠状动脉钙化积分CT为QR36。其余参数均一致:窗宽/窗位345/50,层厚/间隔3 mm/1.5 mm。大螺距肺CT图像作为A组,冠状动脉钙化积分CT图像作为B组。
1.5 钙化积分测量及风险等级分级
A、B组图像分别采用3种方法测量AS:①Syngo.via工作站测量:将图像中CT值>130 HU的区域进行色彩标记,然后由图像后处理技师手动选择冠脉解剖结构后再自动计算得出AS。②AI测量:AI软件包括非门控钙化积分和门控钙化积分两个模块,分别用于测量A组和B组图像。两个模块均采用卷积神经网络的深度学习算法。③AI+手动校正测量:由图像后处理技师在AI测量的基础上,手动调整AI识别的冠状动脉钙化区域,包括增加或删除钙化区域。
Syngo.via工作站测量A、B组图像所得AS分别记录为A1组、B1组;AI非门控钙化积分模块测量A组图像所得AS为A2组,AI非门控钙化积分模块测量+手动校正A组图像所得AS为A3组;AI门控钙化积分模块测量B组图像所得AS为B2组,AI门控钙化积分模块测量+手动校正B组图像所得AS为B3组。对6组钙化积分进行风险分级,分级标准为:1级:小于1,为极低风险;2级:1 ~ 99,为低风险;3级:100 ~ 399,为中度风险;4级:大于400,为高风险。记录A1、A3以及B1、B3的所用时间。
1.6 辐射剂量评估
记录两种检查剂量报告上显示的容积剂量指数(CTDIvol)和剂量长度乘积(DLP)。再根据公式计算有效剂量(ED)。
$$ \mathrm{E}\mathrm{D}=\mathrm{D}\mathrm{L}\mathrm{P}\times 0.014 ^{[7]} $$ 1.7 统计分析
使用SPSS Statistics 27.0软件进行数据分析。连续变量正态分布用
$ \bar{{x}}\pm s $ 表示,非正态分布用M(P25,P75)形式表示。钙化积分作为连续变量,A1和B1组使用配对Wilcox检验评估是否存在统计学差异。A1、A2和A3组之间、B1、A2和A3组之间以及B1、B2和B3组之间分别使用多样本Friedman检验,P<0.05具有统计学差异。如有差异进一步行Nemenyi检验两两比较,P<0.017具有统计学差异(0.017为“Bonferroni校正”调整后的显著性阈值)。并且使用组内相关系数(interclass correlation coefficient,ICC)评估A1、B1组,A1、A2、A3组,B1、A2和A3组以及B1、B2、B3组之间的一致性。一致性较高>0.75;一致性较好0.40 ~ 0.75;一致性较差<0.40。钙化积分风险等级作为分类变量,使用加权Kappa系数来评估A1分别与B1、A2、A3组之间,B1分别与A2、A3、B2、B3组之间风险等级分级的一致性。一致性很强:0.8 ~ 1.0;一致性较强0.6 ~ 0.8;一致性中等0.4 ~ 0.6;一致性一般0.2 ~ 0.4;一致性较差<0.2。A1和A3之间及B1和B3之间所用时间使用配对Wilcox检验评估是否存在统计学差异。2. 结果
2.1 非门控大螺距肺CT与心电门控冠脉钙化积分CT扫描参数和辐射剂量统计(表1)
表 1 两种扫描方法扫描参数和辐射剂量Table 1. Scanning parameters and radiation doses in the two scanning methods扫描方法 实际管电压(kV) 实际管电流(mAs) 容积剂量指数(mGy) 剂量长度乘积(mGy·cm) 有效剂量(mSv) 非门控大螺距肺CT 120(4)* 84-102(4)* 4.0±0.7 149.2±31.2 2.1±0.4 110(13)* 72-104(13)* 100(7)* 102-158(7)* 心电门控冠状动脉
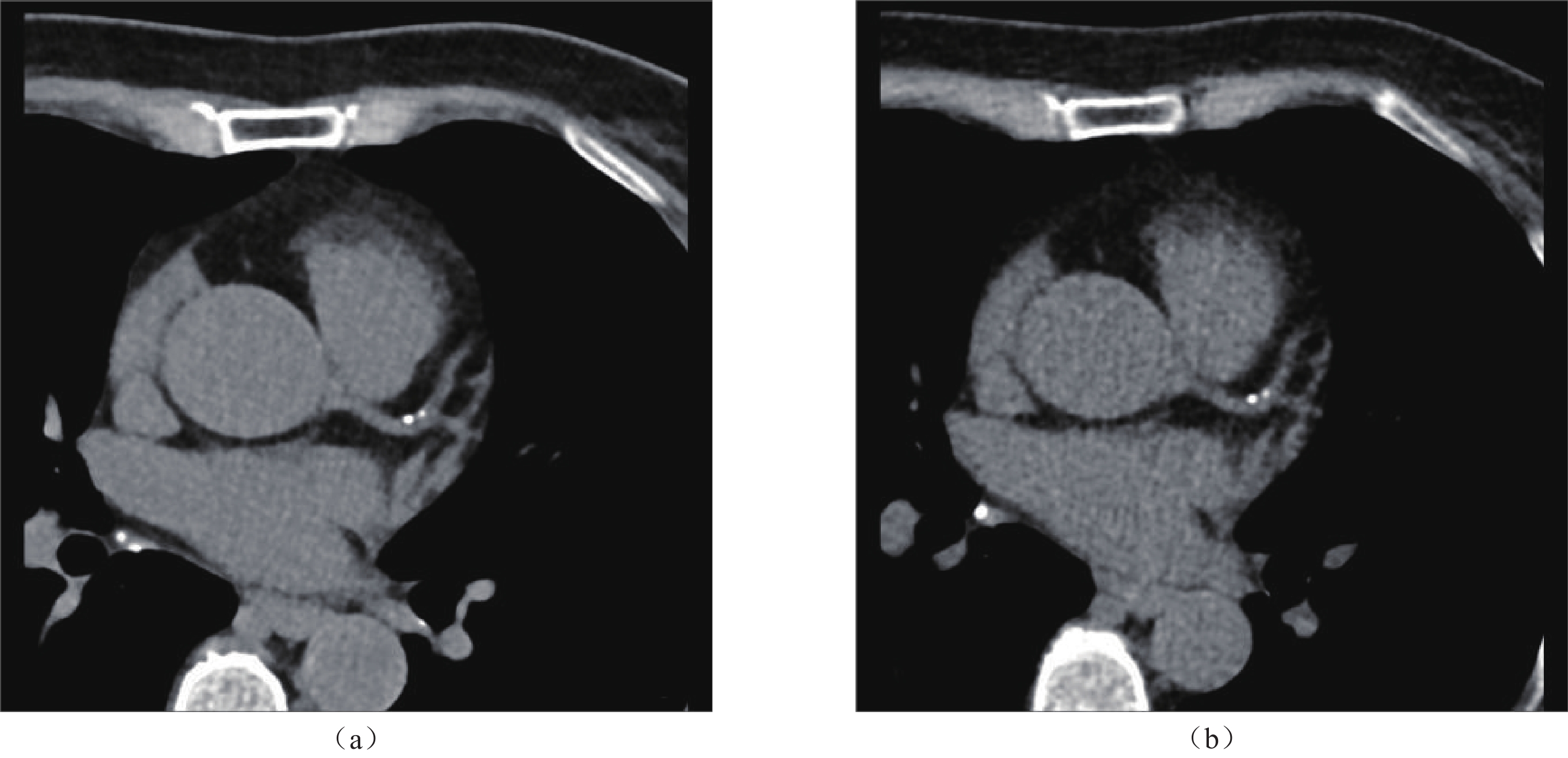
钙化积分CT120(24)* 22-64(24)* 9.0±2.8 152.2±49.2 2.1±0.7 注:*括号内数值代表病例数。 2.2 非门控大螺距肺CT与心电门控冠脉钙化积分CT图像分别使用工作站和AI测量所得钙化积分(表2,图1)
表 2 两种扫描方式图像使用3种测量方法所得钙化积分统计分析Table 2. Calcification scores of the two scanning images using three measurement methods扫描方式 测量方法 Syngo.via
工作站测量AI测量 AI+手动
校正测量X2 P ICC 工作站与AI
测量Kappa工作站与AI+
手动校正
测量Kappa非门控大螺
距肺CT99.70(32.20,374.80) 97.00(31.00,337.00)1 97.50(31.00,351.25)1 27.163 <0.001 0.988
(0.977,0.995)*0.818 0.818 心电门控冠
脉钙化积分CT96.75(30.90,363.40) 90.97(38.59,329.48)2 95.29(30.52,356.43)2 10.900 0.004 0.980
(0.960,0.990)*1.000 1.000 注:1使用AI非门控钙化积分模块测量;2使用AI门控钙化积分模块测量;ICC,组内相关系数;*括号内数值为95%置信空间;Kappa,加权Kappa系数。 2.3 统计分析结果
大螺距肺CT的3种测量方法所得AS有统计学差异,见表2(X2=27.163,P<0.001),对A1、A2和A3组之间使用Nemenyi检验进一步两两比较得出:A1组分别与A2、A3组存在统计学差异(P=0.001、0.011,均<0.017),A2与A3组之间无统计学差异(P=0.107>0.017),A2与A3之间手动校正不为0的共14例,占58%。但AS一致性较高(ICC:0.988)。
心电门控冠脉钙化积分CT使用3种方法测得AS使用多样本Friedman检验时,P=0.004<0.05(表2)。对B1、B2和B3组之间使用Nemenyi检验进一步两两比较得出:B1与B2、B1与B3、B2与B3均无统计学差异(P=0.017、0.900、0.038,均P≥0.017)。因两两比较不存在统计学差异,因此门控冠脉钙化积分CT使用3种方法测得AS不存在统计学差异。B2与B3之间手动校正不为0的共16例,占67%。
大螺距肺CT联合AI(X2=4.795,P=0.091、ICC:0.990)、大螺距肺CT工作站(Z=0.912,P=0.362、ICC:0.988)、门控钙化积分联合AI(X2=10.900,P=0.004、ICC:0.980)分别与门控钙化积分工作站测得AS,均无统计学差异且一致性较高。
非门控大螺距肺CT联合AI及AI+手动校正测量,与门控钙化积分工作站测得AS之间一致性ICC为0.990(0.981,0.995),风险分级Kappa系数:A2与B1、A3与B1之间均为0.925。
A1组与A3组所用时间分别为97(31,337)秒、12.5(5,16.3)秒,存在统计学差异(Z =4.200,P<0.001)。B1组与B3组所用时间分别为32.5(17.3,51.3)秒、15(5,20)秒,存在统计学差异(Z =4.049,P<0.001)。
3. 讨论
随着冠状动脉疾病(CAD)在全球范围内的流行率不断上升,早期诊断和风险评估变得尤为重要。冠状动脉钙化积分(CAC)是评估冠状动脉疾病风险的一个重要指标,已被证明与心血管事件的风险密切相关。非门控肺CT作为一种快速且辐射剂量较低的成像技术,为冠状动脉钙化评估提供了新的方法[8−9],加上AI算法的引入,则进一步提高了CAC评分的自动化和准确性[9−10],为筛查心脏状况提供了一个有价值的工具。常规肺平扫CT[8]及低剂量肺CT[10]已经被证实可以较为准确地测量钙化积分,却仍存在噪声大或存在运动伪影的问题,有时对风险等级产生较大影响。本文通过大螺距联合自动调制技术,在提高时间分辨力、提升图像质量、优化患者辐射剂量(仅约4.0 mGy)的同时,进一步提高钙化积分准确性和风险分级的一致性。
研究结果显示:大螺距肺CT与冠脉钙化积分CT图像使用工作站测量时,钙化积分不存在显著差异,且一致性高达98.8%。相较Budoff[11]与Yu[2]等人研究结果一致性94%和86%,本研究具有更高的一致性。究其原因是大螺距肺CT图像较低剂量肺CT图像质量好,噪声水平低,使得钙化积分测量结果更准确。顾耕[12]等人研究显示,非门控大螺距肺CT平扫与心电门控钙化积分CT所得钙化积分结果有显著差异,并且大螺距肺CT钙化积分值低于门控钙化积分,与本研究结果相反。分析原因,钙化积分CT扫描时采用的前瞻性门控的单一时相(R-R间期75%),而本研究采用了R-R间期35%及75%双时相采集,虽然辐射剂量有所增加,但是可以重建出图像伪影小,冠脉显示更清晰的时相,因此得到了两者无显著差异的结果。此外,本研究中大螺距肺CT图像采集过程中,采用的自动调制技术,实际管电压值并非全为120 kV,约80%患者为100和110 kV,随管电压降低CT值增加,因此大螺距肺CT较门控钙化积分CT所测得的AS高一些,因其影响了钙化积分阈值的测量。但是此变化未对两种采集方式所得AS的差异性(P=0.362)和一致性(ICC:0.988)产生影响,其中仅有3例患者风险分级发生变化,相较门控钙化积分CT的风险分级高出一个等级,但一致性高达0.818。因此可以证明非门控大螺距肺CT代替门控冠状动脉钙化积分CT用于钙化积分评估的可行性。
大螺距肺CT平扫联合AI非门控钙化积分测量模块,通过对大量肺CT图像的反复训练,卷积神经网络的不断学习,建立肺CT测量钙化积分的优质模型。但是研究发现,无论是AI自动或是AI自动+手动校正测量,所得AS与工作站测量都存在差异,且AS出现降低的情况。但大螺距肺CT平扫联合AI与门控钙化积分工作站测量结果相较,并不存在统计学差异。大螺距肺CT图像经过AI训练后所得的AS反倒与门控冠脉钙化积分的工作站测量值更接近。究其原因,可能是AI非门控钙化积分模块在模型训练过程中,以肺CT图像作为输入,以门控钙化积分图像作为预测目标,通过前向传播计算预测结果,然后通过反向传播调整模型参数,因此可以得到与“金标准”(心电门控钙化积分工作站测量结果)更为相近的结果。并且AS一致性高达0.990,风险分级Kappa系数一致性为0.925,以及较工作站测量所用时间显著减少,效率更高。因此大螺距肺CT平扫联合AI保有较高的风险等级诊断效能及临床筛查价值,这与樊荣荣[13]、闫玉辰[14]以及 Andre F[15]等人的研究结论一致。
此外,本研究中心电门控钙化积分CT联合AI,可得到与工作站无差异的结果,且风险分级一致性高达1.000。AS在经过AI+手动校正后的测量结果具有更高的准确性,与陈丽虹[16]与Covas P[17]等人的研究结果一致。
综上所述,非门控大螺距肺CT图像可以用于钙化积分测量,使用AI评估具有较高的准确性,同时降低筛查的辐射剂量,节约检查和诊断时间,可以做到无人为干扰的结果统计,因此具有较高的临床应用价值。而且非门控大螺距肺CT可以使患者少接受冠脉钙化积分扫描中约2.1 mSv的有效剂量、以及约9.0 mGy左右的CTDIvol,尤其针对女性患者,可以大大减低局部辐射剂量,对于扫描范围内的辐射敏感器官-乳腺起到了很好的保护作用。通过一种CT检查,在一次扫描中获取更多的诊疗信息,对心血管疾病的大范围筛查和早诊早治提供了有力保障。
本研究存在的不足之处:(1)样本量较小,无法根据患者自身特征进行分组讨论。(2)本研究所使用成像设备与AI软件源于不同公司,且较为单一,可能会对结果的泛化产生影响。
-
表 1 两种扫描方法扫描参数和辐射剂量
Table 1 Scanning parameters and radiation doses in the two scanning methods
扫描方法 实际管电压(kV) 实际管电流(mAs) 容积剂量指数(mGy) 剂量长度乘积(mGy·cm) 有效剂量(mSv) 非门控大螺距肺CT 120(4)* 84-102(4)* 4.0±0.7 149.2±31.2 2.1±0.4 110(13)* 72-104(13)* 100(7)* 102-158(7)* 心电门控冠状动脉
钙化积分CT120(24)* 22-64(24)* 9.0±2.8 152.2±49.2 2.1±0.7 注:*括号内数值代表病例数。 表 2 两种扫描方式图像使用3种测量方法所得钙化积分统计分析
Table 2 Calcification scores of the two scanning images using three measurement methods
扫描方式 测量方法 Syngo.via
工作站测量AI测量 AI+手动
校正测量X2 P ICC 工作站与AI
测量Kappa工作站与AI+
手动校正
测量Kappa非门控大螺
距肺CT99.70(32.20,374.80) 97.00(31.00,337.00)1 97.50(31.00,351.25)1 27.163 <0.001 0.988
(0.977,0.995)*0.818 0.818 心电门控冠
脉钙化积分CT96.75(30.90,363.40) 90.97(38.59,329.48)2 95.29(30.52,356.43)2 10.900 0.004 0.980
(0.960,0.990)*1.000 1.000 注:1使用AI非门控钙化积分模块测量;2使用AI门控钙化积分模块测量;ICC,组内相关系数;*括号内数值为95%置信空间;Kappa,加权Kappa系数。 -
[1] 周俊林, 萧毅, 张雪君, 等. 中国医学影像人工智能应用现状调研报告[J]. 中华放射学杂志, 2022, 56(11): 1248−1253. DOI: 10.3760/cma.j.cn112149-20220802-00650. ZHOU J L, XIAO Y, ZHANG X J, et al. A survey report on the application status of artificial intelligence in medical imaging in China. Chinese Journal of Radiology, 2022, 56(11): 1248−1253. DOI: 10.3760/cma.j.cn112149-20220802-00650. (in Chinese).
[2] YU J, QIAN L, SUN W, et al. Automated total and vessel-specific coronary artery calcium (CAC) quantification on chest CT: direct comparison with CAC scoring on non-contrast cardiac CT. BMC Med Imaging. 2022 Oct 14;22(1): 177. DOI: 10.1186/s12880-022-00907-1.
[3] CHANG S, REN L, TANG S, et al. Technical note: Exploring the detectability of coronary calcification using ultra-high-resolution photon-counting-detector CT. Med Phys. 2023 Nov;50(11): 6836−6843. DOI: 10.1002/mp.16712.
[4] LLEWELLYN O, WILLIAMS M C. What should we do about Coronary Calcification on Thoracic CT? Rofo. 2022 Aug;194(8): 833−840. English. DOI: 10.1055/a-1752-0577.
[5] JACOBS P C, ISGUM I, GONDRIE M J, et al. Coronary artery calcification scoring in low-dose ungated CT screening for lung cancer: interscan agreement. AJR Am J Roentgenol. 2010 May;194(5): 1244−9. DOI: 10.2214/AJR.09.3047.
[6] PARK S H, HAN K. Methodologic Guide for Evaluating Clinical Performance and Effect of Artificial Intelligence Technology for Medical Diagnosis and Prediction. Radiology. 2018 Mar;286(3): 800−809. DOI: 10.1148/radiol.2017171920.
[7] The 2007 Recommendations of the International Commission on Radiological Protection. ICRP publication 103. Ann ICRP. 2007;37(2−4): 1−332. DOI: 10.1016/j.icrp.2007.10.003.
[8] 孙会利, 陈杰, 张焕, 等. 基于人工智能技术的非门控胸部CT平扫对冠状动脉钙化积分的准确性评价[J]. CT理论与应用研究, 2021, 30(1): 106−113. DOI: 10.15953/j.1004-4140.2021.30.01.11. SUN H L, CHEN J, ZHANG H, et al. Accuracy evaluation of coronary artery calcification score by non gated chest CT scan based on artificial intelligence technology[J]. CT Theory and Applications, 2021, 30(1): 106−113. DOI: 10.15953/j.1004-4140.2021.30.01.11.
[9] LESSMANN N, VAN GINNEKEN B, ZREIK M, et al. Automatic Calcium Scoring in Low-Dose Chest CT Using Deep Neural Networks With Dilated Convolutions. IEEE Trans Med Imaging. 2018 Feb;37(2): 615−625. DOI: 10.1109/TMI.2017.2769839.
[10] LIU Y, CHEN X, LIU X, et al. Accuracy of non-gated low-dose non-contrast chest CT with tin filtration for coronary artery calcium scoring. Eur J Radiol Open. 2022 Jan 17;9: 100396. DOI: 10.1016/j.ejro.2022.100396.
[11] BUDOFF M J, NASIR K, KINNEY G L, et al. Coronary artery and thoracic calcium on noncontrast thoracic CT scans: comparison of ungated and gated examinations in patients from the COPD Gene cohort. J Cardiovasc Comput Tomogr. 2011 Mar-Apr;5(2): 113−8. DOI: 10.1016/j.jcct.2010.11.002.
[12] 顾耕, 陶欣慰, 邓建宏. 无门控大螺距胸部CT扫描心脏冠状动脉钙化积分的可行性研究[J]. 实用放射学杂志, 2022, 38(6): 910−914, 918. DOI: 10.3969/j.issn.1002-1671.2022.06.010. GU G, TAO X W, DENG J H. Coronary artery calcification score detection using thorax CT with TurboFlash mode: a feasibility study. Journal of Practical Radiology, 2022, 38(6): 910−914, 918. DOI: 10.3969/j.issn.1002-1671.2022.06.010. (in Chinese).
[13] 樊荣荣, 刘凯, 夏晨, 等. AI对非门控胸部LDCT平扫冠状动脉钙化积分危险分层的预测价值[J]. 国际医学放射学杂志, 2022, 45(1): 21−26. DOI: 10.19300/j.2022.L18690. FAN R R, LIU K, XIA C, et al. Predictive value of AI in risk stratification of coronary artery calcification score using non-gated chest LDCT. International Journal of Medical Radiology, 2022, 45(1): 21−26. DOI: 10.19300/j.2022.L18690. (in Chinese).
[14] 闫玉辰, 胡磊, 王焰, 等. 基于深度学习技术的非门控胸部CT冠脉钙化积分系统的准确性评价[J]. 放射学实践, 2023, 38(3): 273−278. DOI: 10.13609/j.cnki.1000-0313.2023.03.006. YAN Y C, HU L, WANG Y, et al. Accuracy evaluation of non-gated chest CT coronary calcification scoring system based on deep learning technology. Radiology Practice, 2023, 38(3): 273−278. DOI: 10.13609/j.cnki.1000-0313.2023.03.006. (in Chinese).
[15] ANDRE F, SEITZ S, FORTNER P, et al. Simultaneous assessment of heart and lungs with gated high-pitch ultra-low dose chest CT using artificial intelligence-based calcium scoring. Eur J Radiol Open. 2023 Feb 15;10: 100481. DOI: 10.1016/j.ejro.2023.100481.
[16] 陈丽虹, 郭银霞, 李雅楠, 等. 人工智能冠状动脉钙化积分自动测量方法的临床有效性评估[J]. 实用放射学杂志, 2023, 39(1): 45−48, 69. DOI: 10.3969/j.issn.1002-1671.2023.01.012. CHEN L H, GUO Y X, LI Y N, et al. Clinical effectiveness evaluation of artificial intelligence automatic measurement method for coronary artery calcium score. Journal of Practical Radiology, 2023, 39(1): 45−48, 69. DOI: 10.3969/j.issn.1002-1671.2023.01.012. (in Chinese).
[17] COVAS P, DE GUZMAN E, BARROWS I, et al. Artificial Intelligence Advancements in the Cardiovascular Imaging of Coronary Atherosclerosis. Front Cardiovasc Med. 2022 Mar 21;9: 839400. DOI: 10.3389/fcvm.2022.839400.



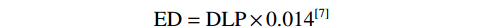
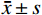
 下载:
下载: