The Predictive Value of CT Findings in Invasive Behavior of Pancreatic Neuroendocrine Tumors
-
摘要: 目的:探讨胰腺神经内分泌肿瘤(pNET)的CT征象对其侵袭性行为的预测价值。方法:回顾性分析经手术病理确诊、临床及CT资料完整、术前均行胰腺CT平扫及增强检查的120例pNET,分析病灶的部位、形态、包膜、有无囊变和钙化、有无胰管扩张、肿瘤的强化方式,测量肿瘤最大径、最短径以及实性部分平扫、动脉期及门脉期密度,并计算动脉期强化差值、门脉期强化差值。根据手术病理结果将肿瘤分为侵袭组和无侵袭组,比较两组间CT征象的差异。使用绘制受试者操作特征(ROC)曲线评价肿瘤最大径、最短径、动脉期差值和门脉期差值对pNET的侵袭性行为的预测价值。结果:侵袭组和无侵袭组pNET在发病部位、胰管扩张、囊变、钙化及强化方式无差异,在形态、完整包膜上有差异。两组在最大径、最短径、动脉期强化差值、门脉期强化差值定量特征有差异,其ROC曲线下面积为0.693、0.69、0.73和0.64,具有判别效能。对6个差异有统计学意义的影像特征通过多变量Logistic回归分析,结果显示动脉期强化差值为判断pNET侵袭性行为的独立预测因素,动脉期强化差值最佳临界点为90.1 HU(灵敏度0.714,特异性0.656,阳性预测值64.5%,阴性预测值72.4%,准确率68.3%)。结论:胰腺神经内分泌肿瘤体积大、形态不规则、包膜不完整或无包膜,肿瘤实性成分动脉期、门脉期强化差值低等征象提示肿瘤具有侵袭性行为,其中动脉期强化差值为pNET侵袭性行为的独立预测因素。Abstract: Objective: To explore the value of CT findings in predicting the invasive behaviors of pancreatic neuroendocrine tumor (pNET). Methods: The clinical data and CT data of 120 patients with pNET confirmed by surgical resection and pathology were retrospectively analyzed. Preoperative CT plain scan and enhanced examination of pancreas were performed. Image analysis included tumor location, shape, capsule, cystic change, calcification, pancreatic duct dilation and enhancement pattern. The maximum and minimum diameter of the tumor were measured. The CT value of the solid part of the tumor was measured in plain scan, arterial phase and portal vein phase. Enhancement difference in arterial phase and portal vein phase were calculated. The tumors were divided into invasive group and non-invasive group according to the pathological results. The difference of CT findings between the two groups was compared. Receivers operating characteristic (ROC) curves were drawn to evaluate the predictive value of tumor maximum diameter, minimum diameter, enhancement difference in arterial phase and portal vein phase on the invasive behavior of pNET. Results: There were no statistical differences in tumor location, pancreatic duct dilation, cystic change, calcification and enhancement pattern between the invasive and non-invasive groups. There were statistically significant differences between the two groups in the quantitative characteristics of the maximum diameter, the minimum diameter, enhancement difference in arterial phase and portal vein phase and the areas under ROC curve were 0.693, 0.69, 0.73 and 0.64, indicating discrimination efficiency. Multivariate Logistic regression analysis of 6 meaningful image features showed that arterial enhancement difference was an independent predictor of pNET invasive behavior, and the optimal critical point of arterial enhancement difference was 90.1HU (sensitivity 0.714, specificity 0.656, positive predictive value 64.5%, negative predictive value 72.4%, accuracy 68.3%). Conclusion <b<:</b< Large volume, irregular shape, incomplete or no capsule of pancreatic neuroendocrine tumor, and low enhancement difference of solid tumor components in arterial and portal phases suggested invasive behavior of tumor, and enhancement difference in arterial phase was an independent predictor of invasive behavior of pNET.
-
Keywords:
- tomography /
- X-ray computer /
- pancreatic neoplasms /
- neuroendocrine tumor
-
胰腺神经内分泌肿瘤(pancreatic neuroendocrine tumor,pNET)是一种十分罕见的肿瘤,起病隐匿,生物学行为表现为高度异质性,既可惰性生长,也可侵袭性生长,甚至发生早期转移,且生物学特性随着疾病的进展而发生变化[1]。近年来,随着检查技术的进步和健康体检的普及,pNET的临床检出率亦呈上升趋势[2]。由于pNET不同的生物学行为,治疗方式及预后也明显不同,因此术前判断肿瘤的侵袭性对临床有重要的指导意义。
以往文献大多数是探讨pNET的CT征象与肿瘤病理分级的相关研究[3-5],很少研究 CT征象对其侵袭性的预测价值,本研究通过分析120例pNET患者的临床及增强CT资料,并结合病理,探讨CT征象对pNET的侵袭性生物学行为的预测价值。
1. 资料与方法
1.1 临床资料
回顾性分析2018年6月至2021年6月上海交通大学医学院附属瑞金医院经手术和病理确诊的pNET患者。纳入标准:①经手术切除病理证实为 pNET,病理资料完整;②手术前 30天内行胰腺CT平扫及增强检查。排除标准:①碘造影剂过敏者;②CT图像肿瘤病灶显示不清;③患者曾有恶性肿瘤史或胰腺手术史。
120例患者中,103例患者为单发病灶、17例多发灶;男58例,女62例,年龄6~80岁。临床上65例患者有不同症状,包括腹痛33例,低血糖症状(如意识障碍、头昏、行为异常以及心慌、心悸和出汗等)22例,其他不典型症状(如恶心、呕吐、纳差以及乏力、腹痛腹胀等)10例。无症状患者55例,在体检或其他原因检查时偶然发现。肿瘤标记物中,神经元特异性烯醇化酶(neuron specific enolase,NSE)异常升高66例,甲胎蛋白(alpha fetoprotein,AFP)异常升高2例,癌胚抗原(carcinoembryonic antigen,CEA)异常升高5例,CA-199异常升高11例,CA125异常升高7例。
1.2 CT检查
120例患者均行胰腺CT平扫及增强扫描,其中,71例采用GE Light Speed VCT 64排螺旋CT,31例采用GE Discovery CT750 HD、18例采用Siemens IQON-SPECTRAL的MDCT设备检查。
由3名具有5年以上工作经验的放射科技师行CT扫描。参数:层厚、间隔5 mm,重建图像层厚l mm,螺距l,管电压120 kV,管电流为自动毫安秒;使用高压注射器经肘部静脉团注非离子型碘造影剂(碘佛醇)1.5 mL/kg,流速为2~3 mL/s,采集2期动态增强CT影像,即增强扫描动脉期(30~35 s)、门静脉期(70~80 s)影像。
1.3 图像评估
CT图像由两名放射科高年资主治医师(参与放射诊断工作≥10年)通过医学影像信息系统(picture archiving and communication systems,PACS)独立进行分析,意见不一致时,由上一级主任医师仲裁得出最终结果。
CT征象的评估:包括病灶部位(胰腺头颈、体、尾部,当肿瘤同时占两个部位时以病灶占据较大位置统计病灶位置)、形态(类圆形或椭圆形、分叶状或不规则形)、包膜(完整、无或不完整)、有无胰管扩张、有无囊变和钙化、肿瘤的强化方式(均匀、不均匀)。
肿瘤大小及CT值的评估:手动测量3次,结果取平均值。包括:①测量肿瘤最大径、最短径;②密度:分别测量平扫、动脉期及门脉期肿瘤实性部分的密度,并计算动脉期差值(动脉期密度与平扫的差值)、门脉期差值(门脉期密度与平扫的差值)。
1.4 统计学分析
采用SPSS 24.0软件进行统计学分析。定性数据以计数表示,使用χ2检验或Fisher确切概率法分析。定量数据使用Kolmogorov-Smirnov测试是否符合正态分布,正态分布资料以
$\bar x\pm s $ 表示,并用独立样本t检验分析。非正态分布的数据用中位数表示四分位范围,使用 Mann-Whitney分析。采用受试者操作特征(receiver operating characteristic,ROC)曲线评价肿瘤最大径、最短径和CT强化指标对pNET侵袭性行为的诊断效能,并计算ROC曲线下面积(area under curve,AUC)、阈值、95% 可信区间(confidence interval,CI)。以差异有统计学意义的CT参数作为协变量进行多变量Logistic回归分析。P<0.05为差异有统计学意义。
2. 结果
2.1 临床及病理资料
依据病理结果(是否侵犯胰腺周围脂肪组织、神经、血管、脾脏、胆总管及胰周淋巴结转移、远处脏器转移等),分为侵袭组(n=64)和无侵袭组(n=56)。侵袭组64例中,侵犯胰周脂肪组织17例,侵犯周围神经5例、脉管癌栓3例,胰周淋巴结转移1例,同时侵犯2个及以上部位38例。
侵袭组与无侵袭组患者在年龄、性别、临床症状、基础疾病方面差异无统计学意义;但肿瘤的分泌功能及病理组织学分级差异有统计学意义。120例pNET中,包括无功能性51例和功能性69例,其中功能性pNET包括胰岛素瘤37例,胃泌素瘤18例,胰高血糖素瘤9例以及生长抑素瘤5例(表1)。
表 1 侵袭组与无侵袭组pNET的临床特征比较Table 1. Comparison of clinical characteristics of pNET between the invasive group and the non-invasive group组别 例数 年龄/岁 性别/例 临床症状
/例基础疾病/例 血清神经元特
异性烯醇化酶
/(ng/mL)分泌功能
/例病理分级
/例男 女 有 无 无 1种 ≥2种 是 否 G1 G2 G3 侵袭组 64 53.72±12.89 33 31 31 33 43 17 4 18.93±6.82 31 33 20 34 10 无侵袭组 56 51.95±14.97 25 31 34 22 44 8 4 30.53±51.13 38 18 38 18 0 统计量 0.485a 0.573b 1.813b 2.730b -1.123 4.609b 20.065b P 0.487 0.470 0.202 0.255 0.261 0.042 <0.001 注:a:t值;b:χ2值。 2.2 CT表现
120例病例均行CT增强扫描,侵袭组和无侵袭组肿瘤在形态、有无包膜、最大径、最短径、肿瘤实性成分动脉期及门脉期强化差值方面有差异,在肿瘤部位、胰管扩张、囊变、钙化、强化方式方面无差异(表2和表3,图1和图2)。
表 2 侵袭组与无侵袭组pNET的CT影像学特征比较结果(例)Table 2. Comparison of CT imaging features of pNET between the invasive group and the non-invasive group (cases)组别 例数 位置 形态 包膜 胰管扩张 囊变 钙化 强化方式 头颈部 体部 尾部 规则 不规则 完整 不完整
或无有 无 有 无 有 无 均匀 不均匀 侵袭组 64 27 12 25 27 37 22 42 21 43 22 42 15 49 24 40 无侵袭组 56 25 15 16 47 9 49 7 13 43 15 41 8 48 25 31 统计值 1.861 22.013 34.889 1.355 0.807 1.615 0.933 P 0.394 <0.001 <0.001 0.311 0.430 0.249 0.354 表 3 侵袭组与无侵袭组pNET的CT影像学特征比较结果Table 3. Comparison of CT imaging features of pNET between the invasive group and the non-invasive group组别 例数 最大径/cm 最短径/cm 肿瘤实性成分强化差值/HU 动脉期差值 门脉期差值 侵袭组 64 4.051±2.920 3.062±2.051 80.933±48.281 73.801±28.912 无侵袭组 56 2.511±1.542 2.084±1.220 112.912±61.953 89.882±39.901 统计检验 统计值 12.518 9.905 10.071 6.501 P 0.001 0.002 0.002 0.012 ![]() 图 1 女,75岁,非侵袭性胰腺神经内分泌肿瘤(a)为CT平扫,示胰头部见一类椭圆形稍低密度灶,密度均匀,边界清。(b)为增强扫描动脉期,示病灶重度强化,强化程度明显高于周围胰腺组织,病灶与胰腺交界面见肿瘤包膜。(c)为增强扫描门脉期,示病灶强化程度不均匀减低,实性部分密度仍高于胰腺组织,分界清,病灶为实性,无囊变坏死。(d)为病理图片,示肿瘤组织呈膨胀性生长,与胰腺组织分界清晰,肿瘤细胞呈器官样排列,细胞形态、大小较一致(HE染色×100)。Figure 1. Female, 75 years old with a non-invasive pancreatic neuroendocrine tumor
图 1 女,75岁,非侵袭性胰腺神经内分泌肿瘤(a)为CT平扫,示胰头部见一类椭圆形稍低密度灶,密度均匀,边界清。(b)为增强扫描动脉期,示病灶重度强化,强化程度明显高于周围胰腺组织,病灶与胰腺交界面见肿瘤包膜。(c)为增强扫描门脉期,示病灶强化程度不均匀减低,实性部分密度仍高于胰腺组织,分界清,病灶为实性,无囊变坏死。(d)为病理图片,示肿瘤组织呈膨胀性生长,与胰腺组织分界清晰,肿瘤细胞呈器官样排列,细胞形态、大小较一致(HE染色×100)。Figure 1. Female, 75 years old with a non-invasive pancreatic neuroendocrine tumor![]() 图 2 女,55岁,侵袭性胰腺神经内分泌肿瘤(a)为CT平扫,示胰尾部见一巨大不规则等密度肿块,密度不均匀,内可见条片低密度影,边界不清。(b)为增强扫描动脉期,示病灶中度不均匀强化,病灶与胰腺交界面未见肿瘤包膜,与周围血管、结肠壁、胃壁分界不清。(c)为增强扫描门静脉期,示病灶实性持续渐进性强化,内见囊变坏死不强化影,病灶以实性成分为主。(d)为病理图片,示肿瘤组织呈浸润性生长,侵犯胰腺周围纤维脂肪组织;肿瘤细胞呈片状排列,细胞大小不一致,部分细胞异型明显,核仁可见(HE染色×100)。Figure 2. Female, 55 years old with a invasive pancreatic neuroendocrine tumor
图 2 女,55岁,侵袭性胰腺神经内分泌肿瘤(a)为CT平扫,示胰尾部见一巨大不规则等密度肿块,密度不均匀,内可见条片低密度影,边界不清。(b)为增强扫描动脉期,示病灶中度不均匀强化,病灶与胰腺交界面未见肿瘤包膜,与周围血管、结肠壁、胃壁分界不清。(c)为增强扫描门静脉期,示病灶实性持续渐进性强化,内见囊变坏死不强化影,病灶以实性成分为主。(d)为病理图片,示肿瘤组织呈浸润性生长,侵犯胰腺周围纤维脂肪组织;肿瘤细胞呈片状排列,细胞大小不一致,部分细胞异型明显,核仁可见(HE染色×100)。Figure 2. Female, 55 years old with a invasive pancreatic neuroendocrine tumor肿瘤的最大径及最短径预测pNET侵袭性行为的ROC曲线的AUC分别为0.693(95%CI 0.598~0.818)、0.690(95%CI 0.594~0.785)(图3);肿瘤实性成分动脉期差值、门脉期差值预测pNET侵袭性行为的ROC曲线的AUC分别为0.730(95%CI 0.642~0.732)、0.640(95%CI 0.530~0.733);结果均显示对pNET的侵袭性行为具有判别效能(图4)。
2.3 利用增强CT定量参数预测pNET的侵袭性行为
筛选出的6个影像学参数(形态、包膜、最大径、最短径、动脉期强化差值、门脉期强化差值)作为变量,以pNET的侵袭性行为为因变量进行多变量Logistic回归分析。Logistic回归方程式为:
$$ y=0.769-0.002\;x ,$$ 其中x为筛选出形态、包膜、最大径、最短径、动脉期强化差值、门脉期强化差值6个影像学参数。
结果显示动脉期强化差值与pNET的侵袭性独立相关(OR=0.25),动脉期强化差值为判断pNET侵袭性行为的独立预测因素(图5),动脉期强化差值最佳临界点为90.1 HU(灵敏度0.714,特异性0.656,阳性预测值64.5%,阴性预测值72.4%,准确率68.3%),动脉期强化差值越小表示肿瘤侵袭性行为风险越高。
3. 讨论
本研究回顾性分析120例pNET患者的临床及增强CT资料,结合手术病理,探讨CT征象对pNET的侵袭性行为的预测价值。结果表明在肿瘤形态、完整包膜、最大径、最短径、动脉期强化差值、门脉期强化差值这6个影像特征方面有差异。通过多变量Logistic回归分析,结果显示动脉期强化差值为判断pNET侵袭性行为的独立预测因素,动脉期强化差值最佳临界点为90.1 HU。
胰腺神经内分泌肿瘤是一种罕见的肿瘤,约占所有胰腺肿瘤的1%~2%[2]。根据细胞的增殖活性包括有丝分裂计数和ki-67指数两项指标,将pNET分为G1、G2和G3三级[3]。肿瘤异质性与肿瘤分级及预后有关[4]。
本研究中,侵袭组G1、G2及G3分别为20例、34例、10例;无侵袭组G1、G2及G3分别为38例、18例、0例;侵袭组与无侵袭组在肿瘤分级方面差异具有统计学意义,提示高级别肿瘤G2/3级更易发生侵袭性行为。有学者研究发现,患者的性别、年龄差异对预测肿瘤分级无统计学意义[4-5],与本研究相符。本研究中侵袭组与无侵袭组患者在临床症状及基础疾病方面差异无统计学意义。本研究结果显示两组在肿瘤部位、胰管扩张、囊变、钙化、强化方式方面差异无统计学意义,Belousova等[6]发现,pNET侵袭组与无侵袭组在肿瘤的部位、囊变、钙化及胰管扩张方面差异无统计学意义,与本研究结果相一致。
根据是否分泌过多激素而产生不同的临床症状,pNET被分为功能性和非功能性。有文献表明无功能性pNET被发现时,约50%~90%为恶性[6-7]。本研究结果显示无功能性pNET(64.7%,33/51)较功能性pNET(44.9%,31/69)更易表现为侵袭性生物学行为,差异有统计学意义,提示无功能性pNET更易表现为侵袭性生物学行为,推测其原因在于无功能pNET通常无临床症状,除非肿瘤增大到压迫或侵犯临近器官并出现症状才发现。
本研究结果显示侵袭组和无侵袭组pNET在大小、形态、包膜方面差异均有统计学意义,肿瘤越大、形态不规则、包膜不完整或无包膜的pNET更具有侵袭性。pNET肿瘤大小、包膜不完整与肿瘤高级别(G2、G3级)、不良预后及转移风险显著相关[6, 8-11];Canellas等[12]研究发现G3级pNET较G1/2级肿瘤更大,肿瘤大于2.0 cm更易发生侵袭性行为。级别越高的肿瘤常浸润生长,容易突破包膜,形成包膜不完整,提示了肿瘤的侵袭性行为。
我们研究发现,肿瘤实性成分在动脉期强化差值、门脉期强化差值方面差异均有统计学意义,非侵袭组肿瘤的实性成分在动脉期、门脉期强化程度及差值明显高于侵袭组,提示非侵袭组肿瘤实性成分血供明显强于侵袭组,推测其原因在于正常胰腺内分泌腺有致密的血管网,分化良好的pNET更可能来自正常的内分泌组织,因此具有密集的血管网络[13-15]。ROC曲线分析结果显示的pNET肿瘤实性部分动脉期及静脉期强化差值曲线下面积分别为0.73和0.64,能较好地预测其侵袭性行为,动脉期强化差值最佳临界点为90.1 HU,动脉期强化差值越小表示肿瘤侵袭性行为风险越高。pNET为血供丰富的肿瘤,其较高的微血管密度(microvascular density,MVD)与高分化pNET显著相关,可预测患者的预后[13]。
我们进一步通过对筛选出的6个差异有统计学意义的影像学参数(形态、包膜、最大径、最短径、动脉期、门脉期强化差值)进行多变量Logistic回归分析,结果显示动脉期强化差值为判断pNET侵袭性的独立预测因素(P=0.001,OR=0.25)。有研究表明,CT增强值对鉴别胰腺神经内分泌肿瘤的病理分级具有价值,病理分级越高的pNET血供越差,影像所见增强后肿瘤的强化程度越低,其中CT动脉早期强化差值越小[5]。Worhunsky等[16]发现动脉期低强化的pNET与肿瘤低分化及不良预后独立相关。这些研究[5,16]都证实了动脉期强化差值在判断pNET分级及预后方面有重要意义,进一步印证了我们的研究结果。
本研究还存在不足:①本研究为回顾性分析,采用的不同 CT机器设备及扫描参数,可能对结果产生一定的影响;②CT在观察肿瘤的包膜、囊变等方面不如MRI的组织分辨率高,在以后的研究中需要结合MRI进行观察;③pNET的G3级病例数相对较少,需要继续收集,以期进一步研究。
综上所述,侵袭性与无侵袭性组pNET在肿瘤形态、完整包膜、最大径、最短径、动脉期强化差值、门脉期强化差值方面存在差异,即肿瘤体积大、形态不规则、包膜不完整或无包膜,肿瘤实性成分动脉期及门脉期强化差值低等征象提示肿瘤具有侵袭性行为,其中动脉期强化差值为判断pNET侵袭性行为的独立预测因素。总之,pNET的一些增强CT特征与侵袭性行为密切相关,这些影像特征对判断肿瘤的侵袭性行为发挥重要作用,在临床工作中具有较强的实用价值。
-
图 1 女,75岁,非侵袭性胰腺神经内分泌肿瘤
(a)为CT平扫,示胰头部见一类椭圆形稍低密度灶,密度均匀,边界清。(b)为增强扫描动脉期,示病灶重度强化,强化程度明显高于周围胰腺组织,病灶与胰腺交界面见肿瘤包膜。(c)为增强扫描门脉期,示病灶强化程度不均匀减低,实性部分密度仍高于胰腺组织,分界清,病灶为实性,无囊变坏死。(d)为病理图片,示肿瘤组织呈膨胀性生长,与胰腺组织分界清晰,肿瘤细胞呈器官样排列,细胞形态、大小较一致(HE染色×100)。
Figure 1. Female, 75 years old with a non-invasive pancreatic neuroendocrine tumor
图 2 女,55岁,侵袭性胰腺神经内分泌肿瘤
(a)为CT平扫,示胰尾部见一巨大不规则等密度肿块,密度不均匀,内可见条片低密度影,边界不清。(b)为增强扫描动脉期,示病灶中度不均匀强化,病灶与胰腺交界面未见肿瘤包膜,与周围血管、结肠壁、胃壁分界不清。(c)为增强扫描门静脉期,示病灶实性持续渐进性强化,内见囊变坏死不强化影,病灶以实性成分为主。(d)为病理图片,示肿瘤组织呈浸润性生长,侵犯胰腺周围纤维脂肪组织;肿瘤细胞呈片状排列,细胞大小不一致,部分细胞异型明显,核仁可见(HE染色×100)。
Figure 2. Female, 55 years old with a invasive pancreatic neuroendocrine tumor
表 1 侵袭组与无侵袭组pNET的临床特征比较
Table 1 Comparison of clinical characteristics of pNET between the invasive group and the non-invasive group
组别 例数 年龄/岁 性别/例 临床症状
/例基础疾病/例 血清神经元特
异性烯醇化酶
/(ng/mL)分泌功能
/例病理分级
/例男 女 有 无 无 1种 ≥2种 是 否 G1 G2 G3 侵袭组 64 53.72±12.89 33 31 31 33 43 17 4 18.93±6.82 31 33 20 34 10 无侵袭组 56 51.95±14.97 25 31 34 22 44 8 4 30.53±51.13 38 18 38 18 0 统计量 0.485a 0.573b 1.813b 2.730b -1.123 4.609b 20.065b P 0.487 0.470 0.202 0.255 0.261 0.042 <0.001 注:a:t值;b:χ2值。 表 2 侵袭组与无侵袭组pNET的CT影像学特征比较结果(例)
Table 2 Comparison of CT imaging features of pNET between the invasive group and the non-invasive group (cases)
组别 例数 位置 形态 包膜 胰管扩张 囊变 钙化 强化方式 头颈部 体部 尾部 规则 不规则 完整 不完整
或无有 无 有 无 有 无 均匀 不均匀 侵袭组 64 27 12 25 27 37 22 42 21 43 22 42 15 49 24 40 无侵袭组 56 25 15 16 47 9 49 7 13 43 15 41 8 48 25 31 统计值 1.861 22.013 34.889 1.355 0.807 1.615 0.933 P 0.394 <0.001 <0.001 0.311 0.430 0.249 0.354 表 3 侵袭组与无侵袭组pNET的CT影像学特征比较结果
Table 3 Comparison of CT imaging features of pNET between the invasive group and the non-invasive group
组别 例数 最大径/cm 最短径/cm 肿瘤实性成分强化差值/HU 动脉期差值 门脉期差值 侵袭组 64 4.051±2.920 3.062±2.051 80.933±48.281 73.801±28.912 无侵袭组 56 2.511±1.542 2.084±1.220 112.912±61.953 89.882±39.901 统计检验 统计值 12.518 9.905 10.071 6.501 P 0.001 0.002 0.002 0.012 -
[1] 吴文铭, 陈洁, 白春梅, 等. 中国胰腺神经内分泌肿瘤诊疗指南(2020)[J]. 中华外科杂志, 2021,59(6): 401−421. DOI: 10.3760/cma.j.cn112139-20210319-00135. WU W M, CHEN J, BAI C M, et al. The Chinese guidelines for the diagnosis and treatment of pancreatic neuroendocrine neoplasms (2020)[J]. Chinese Journal of Surgery, 2021, 59(6): 401−421. DOI: 10.3760/cma.j.cn112139-20210319-00135. (in Chinese).
[2] 敖炜群, 杨光钊, 王健, 等. 非典型胰腺神经内分泌肿瘤的影像学特征[J]. 中华胰腺病杂志, 2020,20(6): 458−461. doi: 10.3760/cma.j.cn115667-20200416-00054 [3] XU W, YAN H, XU L, et al. Correlation between radiologic features on contrast-enhanced CT and pathological tumor grades in pancreatic neuroendocrine neoplasms[J]. The Journal of Biomedical Research, 2020, 35(3): 179−188. DOI: 10.7555/JBR.34.20200039.
[4] OHKI K, IGARASHI T, ASHIDA H, et al. Usefulness of texture analysis for grading pancreatic neuroendocrine tumors on contrast-enhanced computed tomography and apparent diffusion coefficient maps[J]. Japanese Journal of Radiology, 2021, 39(1): 66−75. DOI: 10.1007/s11604-020-01038-9.
[5] KANG J, RYU J K, SON J H, et al. Association between pathologic grade and multiphase computed tomography enhancement in pancreatic neuroendocrine neoplasm[J]. Journal of Gastroenterology and Hepatology, 2018. DOI: 10.1111/jgh.14139.
[6] BELOUSOVA E, KARMAZANOVSKY G, KRIGER A, et al. Contrast-enhanced MDCT in patients with pancreatic neuroendocrine tumours: Correlation with histological findings and diagnostic performance in differentiation between tumour grades[J]. Clinical Radiology: Journal of the Royal College of Radiologists, 2017, 72(2): 150−158. DOI: 10.1016/j.crad.2016.10.021.
[7] BICCI E, COZZI D, FERRARI R, et al. Pancreatic neuroendocrine tumours: Spectrum of imaging findings[J]. Gland Surgery, 2020, 9(6): 2215−2224. DOI: 10.21037/gs-20-537.
[8] PENITENTI F, LANDONI L, SCARDONI M, et al. Clinical presentation, genotype-phenotype correlations, and outcome of pancreatic neuroendocrine tumors in Von Hippel-Lindau syndrome[J]. Endocrine, 2021, 74(1): 180−187. DOI: 10.1007/s12020-021-02752-8.
[9] YANG M, TIAN B, ZHANG Y, et al. Epidemiology, diagnosis, surgical treatment and prognosis of the pancreatic neuroendocrine tumors: Report of 125 patients from one single center[J]. Indian Journal of Cancer, 2015, 52(3): 343−349. DOI: 10.4103/0019-509X.176746.
[10] LI W X, MIAO F, XU X Q, et al. Pancreatic neuroendocrine neoplasms: CT spectral imaging in grading[J]. Academic Radiology, 2021, 28(2): 208−216. DOI: 10.1016/j.acra.2020.01.033.
[11] OKABE H, HASHIMOTO D, CHIKAMOTO A, et al. Shape and enhancement characteristics of pancreatic neuroendocrine tumor on preoperative contrast-enhanced computed tomography may be prognostic indicators[J]. Annals of Surgical Oncology, 2017, 24(5): 1399−1405. DOI: 10.1245/s10434-016-5630-4.
[12] CANELLAS R, BURK K S, PARAKH A, et al. Prediction of pancreatic neuroendocrine tumor grade based on CT features and texture analysis[J]. American Journal of Roentgenology, 2018, 210(2): 341−346. DOI: 10.2214/AJR.17.18417.
[13] GAO H, WANG W, ZHANG W, et al. The distinctive characteristics of the micro-vasculature and immune cell infiltration in cystic pancreatic neuroendocrine tumors[J]. Journal of Endocrinological Investigation, 2021, 44(5): 1011−1019. DOI: 10.1007/s40618-020-01396-1.
[14] JAYSON G C, KERBEL R, ELLIS L M, et al. Antiangiogenic therapy in oncology: Current status and future directions[J]. Lancet, 2016, 388(10043): 518−529. DOI: 10.1016/S0140-6736(15)01088-0.
[15] CHU X, GAO X, JANSSON L, et al. Multiple microvascular alterations in pancreatic islets and neuroendocrine tumors of a Men1 mouse model[J]. American Journal of Pathology, 2013, 182(6): 2355−2367. DOI: 10.1016/j.ajpath.2013.02.023.
[16] WORHUNSKY D J, KRAMPITZ G W, POULLOS P D, et al. Pancreatic neuroendocrine tumours: Hypoenhancement on arterial phase computed tomography predicts biological aggressiveness[J]. The Official Journal of the International Hepato Pancreato Biliary Association, 2014, 16(4): 304−311. DOI: 10.1111/hpb.12139.



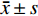
 下载:
下载:








